
【题目】21世纪是钛的世纪.在800℃~1000℃时电解TiO2可制得钛,装置如图所示.下列叙述正确的是( ) 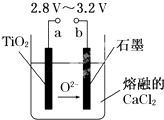
A.a为电源的正极
B.石墨电极上发生还原反应
C.阴极发生的反应为:TiO2+4e﹣═Ti+2O2﹣
D.每生成0.1mol钛,转移电子0.2mol
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:

查阅资料:Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。(Sn: 119)
回答下列问题:
(1) 操作Ⅰ是________、过滤洗涤。
(2)SnCl2粉末需加浓盐酸进行溶解,目的是_______________________________。
(3)加入Sn粉的作用有两个:①调节溶液pH,②____________________________。[
(4)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是___________________。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl![]() SnCl2+ H2↑;
SnCl2+ H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2+ K2Cr2O7+ 14HCl![]() 6FeCl3+ 2KCl + 2CrCl3+7H2O
6FeCl3+ 2KCl + 2CrCl3+7H2O
现取0.80 g锡粉,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液20.00mL。则锡粉中锡的纯度为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可以一次性鉴别氯化钾、盐酸、氢氧化钠三种溶液的试剂是( )
A. 紫色石蕊试液 B. AgNO3溶液 C. Na2CO3溶液 D. BaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】升高温度时,化学反应速率加快原因的合理解释是
A.该化学反应的过程是吸热的
B.该化学反应的过程是放热的
C.分子运动速率加快,使反应物分子的碰撞机会增多
D.反应物分子的能量增加,活化分子百分数增加,有效碰撞次数增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组模拟工业合成氨,并制备NaHCO3,设计实验如下(夹持装置略去)。
回答下列问题:

(1)装置E中盛放碱石灰的仪器名称为_____________________________。
(2)装置A中发生反应的离子方程式为___________________________________________________。
(3)装置C的作用为使N2和H2混合均匀______________________、_________________________。
(4)实验时,应先打开装置B中分液漏斗活塞,反应一段时间,在装置末端导管处收集H2并验纯后,再点燃D处酒精灯,原因为___________________________________________________________。
(5)当F中的氨气饱和后,取下装置F,再向其中通入足量CO2,现象为______________________;发生反应的离子方程式为______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钙是一种阻锈剂,可用于染料工业,某兴趣小组拟制备Ca(NO2)2并对其性质进行探究。
【背景素材】
Ⅰ.NO+NO2+Ca(OH)2Ca(NO2)2+H2O。
Ⅱ.Ca(NO2)2能被酸性KMnO4溶液氧化成![]() ,
, ![]() 被还原为Mn2+。
被还原为Mn2+。
Ⅲ.在酸性条件下,Ca(NO2)2能将I氧化为I2, ![]() 能将I2还原为I。
能将I2还原为I。
【制备氮氧化物】
(1)甲组同学拟利用如下图所示装置制备氮氧化物。
![]()
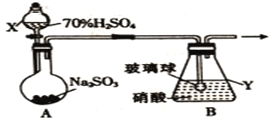
①仪器X的名称是_______________,在制备氮氧化物前要先____________________________。
②装置B中逸出的NO与NO2的物质的量之比为1∶1,则装置B中发生反应的化学方程式为____________________________________________________,若其他条件不变,增大硝酸的浓度,则会使逸出的气体中n(NO2)__________n(NO)(填“>”或“<”)。
【制备Ca(NO2)2】
(2)乙组同学拟利用装置B中产生的氮氧化物制备Ca(NO2)2,装置如图。
![]()
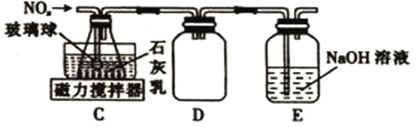
①装置C中导管末端接一多孔玻璃球的作用是______________________________________。
②装置D的作用是_______________________;装置E的作用是______________________。
【测定Ca(NO2)2的纯度】
(3)丙组同学拟用滴定法测定Ca(NO2)2的纯度(杂质不参加反应),可供选择的试剂:
a.稀硫酸 b.c1 mol·L1的KI溶液 c.淀粉溶液
d.c2 mol·L1的Na2S2O3溶液 e.c3 mol·L1的酸性KMnO4溶液
①利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是________________(填字母)。
②利用Ca(NO2)2的氧化性来测定其纯度的步骤:准确称取m g Ca(NO2)2样品放入锥形瓶中,加适量水溶解,加入______________________________,然后滴加稀硫酸,用c2 mol·L1的Na2S2O3溶液滴定至溶液颜色由________________________,且半分钟内不变色,读取消耗Na2S2O3溶液的体积。为减少误差,须__________________________________________(请补充完整实验步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属的防护方法不正确的是 ( )
A.对健身器材涂油漆以防止生锈
B.用牺牲锌块的方法来保护船体
C.对某些工具的“机械转动部位”选用刷油漆的方法来防锈
D.在地下输油的铸铁管上接直流电源的负极来防锈
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com