
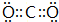 ;
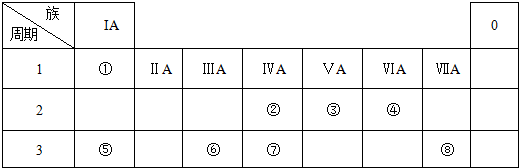
;分析 由元素在周期表中的位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是Cl.
(1)非金属性越强,最高价含氧酸的酸性越强;
(2)③形成的单质为N2,分子中N原子之间形成3对共用电子对;②的最高价氧化物为CO2,碳原子与氧原子之间形成2对共用电子对;⑧的最高价氧化物水化物为Cl2O7,属于分子晶体;
(3)碳与二氧化硅反应生成Si与CO;
(4)利用最高价含氧酸的酸性强弱比较.
解答 解:由元素在周期表中的位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是Cl.
(1)同周期自左而右非金属性增强、同主族自上而下非金属性减弱,非金属性越强,最高价含氧酸的酸性越强,故酸性:HNO3>H2CO3>H2SiO3,
故答案为:HNO3>H2CO3>H2SiO3;
(2)③形成的单质为N2,结构式为N≡N,②的最高价氧化物为CO2,电子式为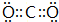 ;⑧的最高价氧化物水化物为Cl2O7,属于分子晶体,
;⑧的最高价氧化物水化物为Cl2O7,属于分子晶体,
故答案为:N≡N;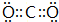 ;分子晶体;
;分子晶体;
(3)碳与二氧化硅反应生成Si与CO,反应方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(4)碳的非金属性弱于Cl元素的,可以利用最高价含氧酸中强酸制备弱酸证明,反应方程式:2HClO4+Na2CO3=2NaClO4+CO2↑+H2O,
故答案为:2HClO4+Na2CO3=2NaClO4+CO2↑+H2O.
点评 本题考查元素周期表与元素周期律综合应用,熟练掌握元素周期表的结构,掌握金属性、非金属性强弱比较实验事实.


科目:高中化学 来源: 题型:选择题
| A. | 25℃时,100mLPH=1的CH3COOH溶液中含有的H+总数大于0.01NA | |
| B. | 标准状况下,11g3H216O种含有的质子数为6NA | |
| C. | 1molLi2O和Na2O2的混合物中含有的离子总数为3NA | |
| D. | 1molN2与足量H2混合,充分反映后转移电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
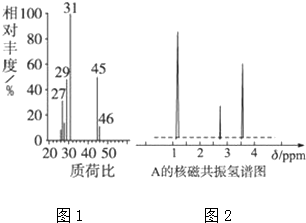
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
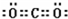 ;E的单质在空气中燃烧所生成物质的化学式SO2.
;E的单质在空气中燃烧所生成物质的化学式SO2.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯能与浓硝酸浓硫酸反应生成三硝基甲苯 | |
| B. | 1 mol甲苯能与3 mol H2发生加成反应 | |
| C. | 甲苯能使酸性高锰酸钾褪色 | |
| D. | 甲苯能燃烧产生带浓烟的火焰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com