
��15�֣�
��һ���������ᣬ��һ���¶��´ﵽ����ƽ��ʱ��������Ũ�ȴ���һ�ֶ����Ĺ�ϵ���±�Ϊ����������25��ʱ�ĵ���ƽ�ⳣ��
�� | ����ƽ�ⳣ��K |
|
|
|
|
|
|
�ش��������⣺
��1��Kֻ���¶��йأ����¶�����ʱ��Kֵ____�����������С���������䡱����
��2���ӵ���ĽǶȣ�HCO3-��HPO42-��H2PO4-���ɿ������ᣬ����������ǿ����_________����������________��
��3������ͬһ�ֶ�Ԫ���ᣬ�в�ֹһ������ƽ�ⳣ�����������K1��K2��K3��֮�����ij�ִ�С��ϵ���˹�ϵ��________________����̼��Ϊ���������ӷ���ʽ�ͱ�Ҫ������˵�������˹��ɵ�ԭ��_________________________��
��4������ƽ�ⳣ������ʵ��ķ����ⶨ�����ģ����Ѿ����25��ʱ��c mol/L��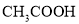 �ĵ���ת����Ϊ____������¶��´���ĵ���ƽ�ⳣ��
�ĵ���ת����Ϊ____������¶��´���ĵ���ƽ�ⳣ��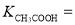 _____��
_____��
������������SOCl2��һ��Һ̬������е�77 �档��ʢ��10 mLˮ����ƿ�У�С�ĵصμ�8��10��SOCl2���ɹ۲쵽���ҷ�Ӧ��Һ�����а����γɣ����д��̼�����ζ�������ݳ����������ʹ����Ʒ����Һ����ֽ��ɫ��
��1��д��SOCl2��ˮ��Ӧ�Ļ�ѧ����ʽ��_____________________________��
��2����AlCl3��Һ���ɡ����գ����õ�����Ҫ��������� ����SOCl2��AlCl3��6H2O��Ϲ��ȵõ���ˮAlCl3��ԭ����________________________ ��
��һ����1������ ��2��H2PO4-��HPO42-
��3��K1>K2>K3��1�֣�����Ԫ����ֲ����룬��һ�����������H+������һ���ĵ��룬����̼��Ķ������볣��С��һ�����볣����H2CO3 H+ + HCO3- ��HCO3-
H+ + HCO3- ��HCO3- H+ + CO32-
H+ + CO32-
��4��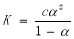
��������1��SOCl2+H2O = SO2��+2HCl
��2��Al2O3
��Ϊ����SOCl2��Ϲ���ʱ������SOCl2������ˮ����ֹAlCl3��ˮ�⣬ͬʱ������HClҲ��������AlCl3��ˮ�⡣
��������
�����������1��������ʵĵ��������ȷ�Ӧ�������¶ȴٽ�������ʵ��룬��������Ũ������Ӧ��Ũ�ȼ�С������Kֵ���ʴ�Ϊ������
��2������ƽ�ⳣ��Խ�������Խǿ��ԽС������Խ�������ݱ���֪��������ǿ����H2PO4-���������� HPO42-���ʴ�Ϊ��H2PO4-��HPO42-��
��3����Ԫ����ֲ����룬��һ������̶���ڶ��������������μ�С��ԭ������һ�����������H+����һ���������������ã���̼��Ϊ����̼��Ķ������볣��С��һ�����볣����H2CO3 H+ + HCO3- ��HCO3-
H+ + HCO3- ��HCO3- H+ + CO32- ��
H+ + CO32- ��
��4��������Һ��ˮ�������������Ũ�Ⱥ�С�����ڴ�����������������˵ˮ������������ӿ��Ժ��ԣ����Ը���Һ��c��CH3COO-��=c��H+��=c ��mol/L����Һ��c��CH3COOH��=c��1-����mol/L��
�����ƽ�ⳣ��K=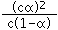 =
=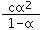 ���ʴ�Ϊ��
���ʴ�Ϊ��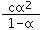 ��
��
��������1�����ݷ�Ӧ�������������Ϊ�д̼�����ζ�Ķ���������Ȼ������壻SOCl2��ˮ��Ӧ���ɵ��Ȼ������Ȼ���ˮ�����������ã���Ӧ�Ļ�ѧ����ʽΪ��SOCl2+H2O=2HCl��+SO2����
��2������AlCl3��Һ���ܵõ���ˮAlCl3����Ϊ����AlCl3��Һʱ������AlCl3ˮ�����ɵ�HCl�ӷ������õ�Al(OH)3���������ջ����Al2O3����ʹSOCl2��AlCl3?6H20��ϲ����ȣ��ɵõ���ˮAlCl3��SOCl2��ˮ��Ӧ���ɵ��Ȼ������Ȼ���ˮ�����������ã�
�ʴ�Ϊ��SOCl2+H2O=2HCl��+SO2������Ӧ�������Ȼ�����������������ӵ�ˮ�⣻
���㣺����ˮ��ƽ�⼰������ʵĵ���ƽ��͵���ȡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�߶���ѧ�����п��ԣ�������ѧ�Ծ��������棩 ���ͣ�ѡ����
����1L 0.1 mol��L-1 NH4Cl��Һ����ȷ����
A����Һ�ʼ���
B��ͨ������HCl��c(NH4��)��c(Cl��)������
C����Һ�к���NH4����ĿΪ0.1NA��NA��ʾ�����ӵ���������ֵ��
D�������¶ȣ���ҺpH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�߶���ѧ�����п��ԣ��ģ���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڢ�KOH����Al(OH)3 ����H2SO4���������У������������������Һ���ܷ�Ӧ����
A���ں͢� B���٢ڢ� C���ٺ͢� D��ֻ�Т�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�߶���ѧ�����п��ԣ��ģ���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������У����÷�Һ©�����з������
A�����Ȼ�̼��Һ�� B�����ͺͻ�����
C������ʳ��ˮ D���ƾ���ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�߶���ѧ�����п��ԣ��ģ���ѧ�Ծ��������棩 ���ͣ�ѡ����
������������ֱ�Ӽ��ȵ���
A.��Ͳ B.����ƿ C.�Թ� D.�ձ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�����и߶���ѧ�����п��Ի�ѧ�������Ծ��������棩 ���ͣ�ѡ����
��������ʵ���ó��Ľ��ͻ������ȷ����
ѡ�� | ʵ����ʵ | ���ͻ���� |
A | �������Ʊ�Һ�ζ�ʳ�IJ�����,�ü�����ָʾ���������� | ǡ����ȫ�к�ʱ��Һ�ʼ��ԣ� Ӧѡ�÷�̪��ָʾ�� |
B | ѹ����Ͳ�ڵ�NO2��N2O4������壬 ��ɫ�ȱ�����dz | ����ѹǿ��ƽ��������N2O4�ķ����ƶ�����ƽ��Ⱦ�ƽ��ѹǿС |
C | ���Ȼ�����Һ�м����Ȼ������壬��Һ��ɫ���� | ˮ��ƽ�������ƶ�����������Ũ�������Ȼ���ˮ��̶����� |
D | �����������Է����з�Ӧ:(NH4)2CO3 (s) = NH4HCO3 (s)+NH3(g) ��H >0 | ����һ�������ķ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�����и߶���ѧ�����п��Ի�ѧ�������Ծ��������棩 ���ͣ�ѡ����
SF6��һ�������ľ�Ե���壬���ӽṹ��ֻ����S-F������֪��1molS(s)ת��Ϊ��̬��ԭ����������280kJ������1molF-F ��S-F�������յ������ֱ�Ϊ160kJ��330kJ����S(s)��3F2(g)=SF6(g)�ķ�Ӧ�Ȧ�HΪ
A��?1780kJ/mol B��?1220 kJ/mol
C��?450 kJ/mol D��+430 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�����и߶���ѧ�����п��Ի�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
����ʵ���У���ɫû�з������Ա仯����
A��������Һ�м���ϡ����
B���������м���Ũ����
C��������Һ�м�����
D����������Һ������������ͭ��Һ��ϼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�����и߶���ѧ�����п��Ի�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
̼Ԫ�ؿ��Դ�������Ȼ��Ķ��������У���Щ���ʿ϶�������
A��ʯ�� B��ʯ��ʯ C����Ȼ�� D��ʯӢɰ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com