
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
���� ���ʷ�����ѧ��Ӧ��������Ӽ䷢����Ч��ײ����ͨ���Ӽ�IJ��ܷ�����Ч��ײ����ѧ��Ӧ��ʵ���Ǿɼ��Ķ��Ѻ��¼����γɣ���ԭ�ӵ�������ϣ�Ҳ�Ǿɻ�ѧ���Ķ��Ѻ��»�ѧ�����γɹ��̣���ѧ��Ӧ��ʵ���Ǿɻ�ѧ���Ķ��Ѻ��»�ѧ�����γɹ��̣���������к���ȡ��ʱ����Ч��ײ��ע������ѹǿ������ı�Ũ�ȣ���Ӧ���ʲŷ����仯���ݴ˷������
��� �⣺�ٻ���Ӽ��к��ʵ�ȡ��������ײ���ܷ�����ѧ��Ӧ���ʢٴ���
����ͨ���Ӽ䲻���ܷ�����ѧ��Ӧ���ʢڴ���
������Ӧ��Ũ�ȣ�����Ӱٷ������䣬��Ũ�����ʢ۴���
������ѹǿ��Ũ����������Ӱٷ������䣬�ʢܴ���
�ݻ�ѧ��Ӧ��ʵ���Ǿɻ�ѧ���Ķ��Ѻ��»�ѧ�����γɹ��̣������ȳ�Ϊ����ӣ�����ӷ�����ײ�������������ʣ��ʢ���ȷ��
�����ɽ��ͻ�ܣ����������Ӱٷ���������Ӧ���ʣ��ʢ���ȷ��
��ѡB��
���� ���⿼�黯ѧ��Ӧ����Ӱ�����ء���ѧ��Ӧʵ�ʵ�֪ʶ�㣬��ȷ��ѧ��Ӧ����Ӱ������ԭ���ǽⱾ��ؼ���֪����Щ�����ܸı�����Ũ�ȡ���Щ�����ܸı����Ӱٷ�������Ŀ�ѶȲ���


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����



| A�� | �٢ڢۢܢ� | B�� | �ڢܢ� | C�� | �ۢݢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ | B�� | ���� | ||
| C�� | ���Ը��������Һ | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
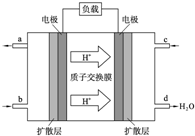 ����Ӧ��ԭ���ԭ�������˶��ֵ�������㲻ͬ����Ҫ����ط�����Խ��Խ��Ҫ�����ã���������ɴ����������ǡ����ԡ�������ȣ����벻����ʽ�����ĵ�أ�ͬʱ�����ĵ����㶪��Ҳ��Ի��������Ⱦ������������ṩ����Ϣ���ش��������⣺
����Ӧ��ԭ���ԭ�������˶��ֵ�������㲻ͬ����Ҫ����ط�����Խ��Խ��Ҫ�����ã���������ɴ����������ǡ����ԡ�������ȣ����벻����ʽ�����ĵ�أ�ͬʱ�����ĵ����㶪��Ҳ��Ի��������Ⱦ������������ṩ����Ϣ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
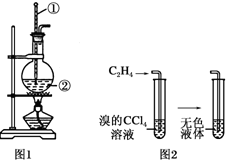 ��ͼ��ʵ��������ϩ�ķ���װ�ú���ϩ����ʵ��װ�ã���Ӧԭ��Ϊ��
��ͼ��ʵ��������ϩ�ķ���װ�ú���ϩ����ʵ��װ�ã���Ӧԭ��Ϊ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� | �� | |
| �� | �� | �� |
| A�� | ԭ�Ӱ뾶������������ | B�� | �������������ף��� | ||
| C�� | �����ԣ��ף��� | D�� | ����������ԣ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1-��ϩ | B�� | 1��3-���ױ� | ||
| C�� | �ױ� | D�� | 2-��-3-�һ�-2-��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO��g��+$\frac{1}{2}$O2 ��g���TCO2��g����H=-283 kJ/mol | |
| B�� | CH4��g��+2O2��g���TCO2��g��+2H2O ��g����H=-802.3 kJ/mol | |
| C�� | 2H2��g��+O2��g���T2H2O ��l����H=-571.6 kJ/mol | |
| D�� | H2 ��g��+Cl2 ��g���T2HCl ��g����H=-184.6 kJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com