

分析 (1)依据三价铁离子的氧化性和硫化氢的还原性来分析,依据流程关系图分析,在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,操作Ⅱ加入稀硫酸调节溶液PH=2为了除去杂质离子Sn2+;
(2)操作IV的目的是从滤液中析出绿矾晶体,利用蒸发浓缩,结晶洗涤得到晶体;
(3)操作IV得到的绿矾晶体用少量冰水洗涤目的是洗去表面杂质,温度降低绿矾溶解度降低,减少绿矾晶体的损失;
(4)①滴定操作中正确的操作方法是左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化;
②当溶液里有Fe2+时,滴入的酸性高锰钾紫色溶液立即裉色,当溶液里没有Fe2+时,滴入的酸性高锰酸钾溶液紫色不褪去,结合这二种现象确定终点判断;
③因为Fe2+还原性很强,在滴定过程中也有可能被空气中的氧气氧化,另外还有可能本身样品中就含有一定的杂质.
解答 解:(1)Fe3+有强氧化性,H2S有强还原性,二者相遇要发生氧化还原反应,发生反应的离子方程式为2Fe3++H2S=Fe2++S↓+2H+,在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5,在溶液PH=2时,Sn2+完全沉淀,亚铁离子不沉淀,
故答案为:2Fe3++H2S=Fe2++S↓+2H+;使Sn2+沉淀完全,防止Fe2+生成沉淀;
(2)滤液中得到晶体,需要对溶液进行加热蒸发浓缩,结晶析出,过滤洗涤等,所以操作IV的顺序依次为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:蒸发浓缩;冷却结晶;
(3)冰水温度低,物质溶解度减小,可以洗去沉淀表面的杂质离子,避免绿矾溶解带来的损失,故答案为:降低洗涤过程中FeSO4•7H2O的损耗;
(4)①滴定时为准确判断滴定终点,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化,故答案为:锥形瓶中溶液颜色的变化;
②当溶液里有Fe2+时,滴入的酸性高锰钾紫色溶液立即裉色,当酸性高锰酸钾溶液过量是溶液会显紫色,故滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色为滴定终点,故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
③用上述方法测定的样品中FeSO4•7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因是洗涤不彻底,亚铁离子被空气中的氧气部分氧化,故答案为:样品中存在少量的杂质或样品部分被氧化.
点评 本题考查了铁盐亚铁盐的性质应用,分离混合物的实验方法设计和分析判断,滴定实验的分析判断,数据计算,误差分析的方法,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 常温时56g铁片投入足量浓硫酸中生成NA个SO2分子 | |
| B. | 12g石墨和C60的混合物中质子总数一定为6NA个 | |
| C. | 25℃,pH=12的Na2CO3溶液中含有CO32-的数目为0.01NA | |
| D. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 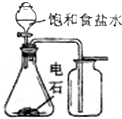 实验室制备并收集乙炔 | B. | 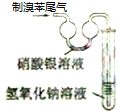 证明溴苯中含溴元素 | ||
| C. | 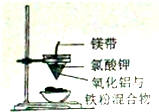 铝热反应 | D. | 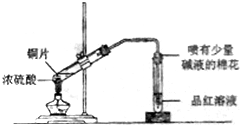 检测铜与浓硫酸反应的气体产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环已醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环已烯 | 0.81 | -103 | 83 | 难溶于水 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同体积、相同密度的CO和C2H4 | |
| B. | 相同质量、不同密度的N2和C2H4 | |
| C. | 相同压强、相同体积、相同质量的O2和N2 | |
| D. | 相同温度、相同压强、相同体积的O2和N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com