
下列各项表述正确的是 ( )
A.水分子的结构式是H—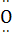 —H
—H
B.NaCl的电子式为N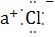
C.23Na37Cl中质子数和中子数之比是7∶8
D.三氟化氮的电子式为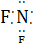 F
F
科目:高中化学 来源: 题型:
为解决日益加剧的温室效应等问题,科学家正在研究建立如下图所示的二氧化碳新循
环体系:
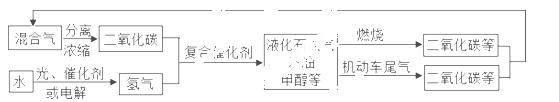
上述关系图能反映的化学观点或化学思想有:( )
①化学变化中元素种类是守恒的;②燃烧时化学能可以转化为热能和光能;③光能或电能可以转化为化学能;④无机物和有机物可以相互转化;⑤二氧化碳也是一种重要的资源.
A.①②③ B.①②④⑤ C.①④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在 500℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和 。
(2)为检验分解产物的成份,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
① A中固体充分加热较长时间后,通入氮气,目的是 。
②为验证A中残留物是否含有FeO,需要选用的试剂有 。
A.KSCN溶液 B.稀硫酸
C.浓盐酸 D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有 气体生成,若含有该气体,观察到的现象为 。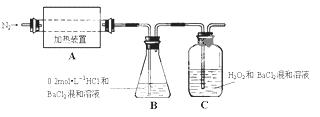
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则b a(填“大于”、“小于”或“等于”)
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为
(用离子方程式表示)。
(3)已知亚铁离子被氧气氧化的反应是:4Fe2+ + O2 + (4+2x) H2O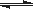 2Fe2O3•xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
2Fe2O3•xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是 ( )
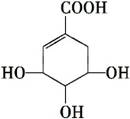
莽草酸
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法中,不正确的是 ( )
A.淀粉、油脂、蛋白质在一定条件下都能发生水解反应
B.“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
C.除去乙酸乙酯中残留的乙酸、乙醇,可加过量饱和Na2CO3溶液振荡后,静置分液
D.淀粉遇碘酒变蓝色,葡萄糖能与新制Cu(OH)2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
元素A的阳离子aAm+与元素B的阴离子bBn-具有相同的电子层结构。以下关于A、B元素性质的比较中,正确的是 ( )
①原子序数:A>B
②离子半径:aAm+<bBn-
③原子半径:A<B
④元素所在的周期序数:A>B
⑤A的最高正价与B的最低负价的绝对值相等
⑥b=a+m-n
A.②③④ B.①②④
C.④⑤⑥ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是 ( )
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合绿色化学原子经济性要求的是 ( )
A.乙烯发生加聚反应制得聚乙烯高分子材料
B.用甲烷与氯气制备一氯甲烷
C.用苯和液溴为原料制取溴苯
D.用石灰石和稀盐酸反应制得二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的反应热等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/ kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列两组物质的熔点高低(填“>”或“<”):
SiC Si,Si SiO2。
(2)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)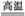 Si(s)+4HCl(g),(已知1 mol Si中含有2 mol Si—Si键)则2 mol H2生成高纯硅需 (填“吸收”或“放出”)能量 kJ。
Si(s)+4HCl(g),(已知1 mol Si中含有2 mol Si—Si键)则2 mol H2生成高纯硅需 (填“吸收”或“放出”)能量 kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com