
¹¤ŅµÉĻŅ²æÉŅŌÓĆCO2ŗĶH2·“Ó¦ÖĘµĆ¼×“¼”£ŌŚ2”Į105Pa”¢300”ęµÄĢõ¼žĻĀ£¬ČōÓŠ44g CO2Óė6g H2Ē”ŗĆĶźČ«·“Ӧɜ³ÉĘųĢå¼×“¼ŗĶĖ®£¬·Å³ö49.5kJµÄČČĮ攣ŹŌŠ“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
ij“ĪŹµŃ齫6molCO2ŗĶ8molH2³äČė2LµÄĆܱÕČŻĘ÷ÖŠ£¬²āµĆH2µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆČēĻĀĶ¼ĖłŹ¾£ØŹµĻߣ©”£
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©aµćÕż·“Ó¦ĖŁĀŹ £ØĢī“óÓŚ”¢µČÓŚ»ņŠ”ÓŚ£©Äę·“Ó¦ĖŁĀŹ”£
£Ø2£©ĻĀĮŠŹ±¼ä¶ĪĘ½¾ł·“Ó¦ĖŁĀŹ×ī“óµÄŹĒ £¬×īŠ”µÄŹĒ ”£
A£®0”«1min
B£®1”«3min
C£®3”«8min
D£®8”«11min
£Ø3£©¼ĘĖćøĆŹµŃéĘ½ŗāŹ±ĒāĘųµÄ×Ŗ»ÆĀŹŗĶøĆĢõ¼žĻĀ·“Ó¦µÄĘ½ŗā³£ŹżK£ØŠ“³ö¼ĘĖć¹ż³Ģ£©”£
£Ø4£©½öøıäijŅ»ŹµŃéĢõ¼žŌŁ½ųŠŠĮ½“ĪŹµŃ飬²āµĆH2µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆČēĶ¼ÖŠŠéĻßĖłŹ¾£¬ĒśĻßI¶ŌÓ¦µÄŹµŃéĢõ¼žøıäŹĒ £¬ĒśĻßII¶ŌÓ¦µÄŹµŃéĢõ¼žøıäŹĒ ”£
CO2(g)+3H2(g) = CH3OH(g)+H2O(g) ”÷H= £49.5kJ”¤mol-1
£Ø3·Ö£¬·½³ĢŹ½2·Ö£¬”÷HµÄ±ķŹ¾1·Ö£¬»ÆѧŹ½”¢×“Ģ¬“ķĪó0·Ö£»£”¢ģŹ±äŹżÖµ”¢µ„Ī»“ķĀ©ŗĻæŪ1·Ö£»¼ĘĮæŹżÓĆ·ÖŹż±ķŹ¾ÓėģŹ±äĻąĘ„ÅäŅ²øų·Ö£©
£Ø1£©“óÓŚ £Ø2·Ö£© £Ø2£©A£Ø1·Ö£©£¬ D £Ø1·Ö£©
£Ø3£©
CO2£Øg£©£«3H2£Øg£© CH3OH£Øg£©£«H2O£Øg£©
CH3OH£Øg£©£«H2O£Øg£©
ĘšŹ¼ĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 3 4 0 0
×Ŗ»ÆĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 1 3 1 1
Ę½ŗāĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 2 1 1 1 £Ø1·Ö£©
H2µÄ×Ŗ»ÆĀŹ=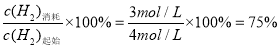 »ņ0.75
»ņ0.75
£Ø2·Ö£¬ÓĆ·ÖŹż±ķŹ¾æŪ1·Ö, “śČėŹżÖµ²»“ųµ„Ī»²»æŪ·Ö£¬²»æ¼ĀĒÓŠŠ§Źż×Ö£©
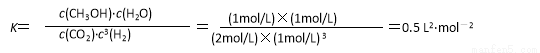 £Ø3·Ö£©
£Ø3·Ö£©
£ØĘäÖŠĮŠŹ½1·Ö£¬“śČėŹżÖµ1·Ö£¬½į¹ū1·Ö£»½į¹ū”¢µ„Ī»“ķĪóŗĻæŪ1·Ö£¬“śČėŹżÖµ²»“ųµ„Ī»²»æŪ·Ö£¬KÖµ²»“ųµ„Ī»²»æŪ·Ö£¬²»æ¼ĀĒÓŠŠ§Źż×Ö£©
£Ø4£©ÉżøßĪĀ¶Č£Ø2·Ö£© Ōö“óŃ¹Ēæ£Ø2·Ö£©
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗŅŃÖŖ4.4g CO2ĘųĢåÓėH2¾“߻ƼÓĒāÉś³ÉCH3OHĘųĢåŗĶĖ®ÕōĘųŹ±·Å³ö4.95kJµÄÄÜĮ棬Ōņ1mol¶žŃõ»ÆĢ¼Č«²æ·“Ó¦·ÅČČ49.5KJ£»½įŗĻČČ»Æѧ·½³ĢŹ½ŹéŠ“·½·ØŠ“³öČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO2£Øg£©+3H2£Øg£©=CH3OH£Øg£©+H2O£Øg£©”÷H=-49.5KJ/mol£»
¹Ź“š°øĪŖ£ŗCO2£Øg£©+3H2£Øg£©=CH3OH£Øg£©+H2O£Øg£©”÷H=-49.5KJ/mol£»
£Ø1£©øł¾ŻĶ¼ĻóæÉÖŖ£¬aµ½b¹ż³ĢÖŠĒāĘųµÄĪļÖŹµÄĮæ¼õŠ”£¬ĖµĆ÷·“Ó¦Ļņ×ÅÕżĻņŅĘ¶Æ£¬Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬
¹Ź“š°øĪŖ£ŗ“óÓŚ£»
£Ø2£©ÓÉĶ¼1æÉÖŖ£¬0”«1minÄŚĒāĘųµÄ±ä»ÆĮæĪŖ8mol-6mol=2mol£» B£®1”«3minÄŚĒāĘųµÄ±ä»ÆĮæĪŖ6mol-3mol=3mol£¬Ę½¾ł1min±ä»ÆĮæĪŖ1.5mol£» C£®3”«8minÄŚĒāĘųµÄ±ä»ÆĮæĪŖ3mol-2mol=1mol£¬Ę½¾ł1min±ä»ÆĮæĪŖ0.2mol£»D£®8”«11min“ļĘ½ŗāדĢ¬£¬ĒāĘųµÄĪļÖŹµÄĮæ²»ŌŁ±ä»Æ£®¹Ź1”«3minĖŁĀŹŌö“ó£¬8”«11minĖŁĀŹ×īŠ”£¬
¹Ź“š°øĪŖ£ŗA£»D£»
£Ø3£©ÓÉĶ¼ĻóæÉÖŖ£¬ŹµĻß±ķŹ¾µÄĒśĻߣ¬ŌŚ8·ÖÖÓ“ļµ½Ę½ŗāדĢ¬£¬“ĖŹ±ĒāĘųµÄĪļÖŹµÄĮæĪŖ2mol£¬ĒāĘųµÄÅضČĪŖ£ŗ2/2=1mol/LĒāĘųµÄÅØ¶Č±ä»ÆĪŖ£ŗ8/2¼õČ„1µČÓŚ3mol·“Ó¦Ē°¶žŃõ»ÆĢ¼µÄÅضČĪŖ£ŗ6/2=3mol/LĄūÓĆ»ÆŃ§Ę½ŗāµÄČż¶ĪŹ½æɵĆ,
CO2£Øg£©£«3H2£Øg£© CH3OH£Øg£©£«H2O£Øg£©
CH3OH£Øg£©£«H2O£Øg£©
ĘšŹ¼ĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 3 4 0 0
×Ŗ»ÆĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 1 3 1 1
Ę½ŗāĪļÖŹµÄĮæÅØ¶Č£Ømol /L£© 2 1 1 1 £Ø1·Ö£©
H2µÄ×Ŗ»ÆĀŹ=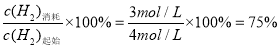 »ņ0.75
»ņ0.75
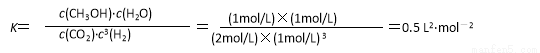
£Ø4£©¶ŌÓŚæÉÄę·“Ó¦CO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©”÷H=-49.0kJ?mol-1£¬Õż·“Ó¦ŹĒĢå»ż¼õŠ”µÄ·ÅČČ·“Ó¦£»ÓÉĶ¼1æÉÖŖ£¬ĒśĻߢń×īĻȵ½“ļĘ½ŗā£¬Ę½ŗāŹ±ĒāĘųµÄĪļÖŹµÄĮæŌö“󣬹ŹøıäĢõ¼žÓ¦Ōö“ó·“Ó¦ĖŁĀŹĒŅĘ½ŗāĻņÄę·“Ó¦ŅĘ¶Æ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ĪŖ£ŗÉżøßĪĀ¶Č£»ĒśĻߢņµ½“ļĘ½ŗāµÄŹ±¼ä±ČŌĘ½ŗā¶Ģ£¬Ę½ŗāŹ±ĒāĘųµÄĪļÖŹµÄĮæ¼õŠ”£¬¹ŹøıäĢõ¼žÓ¦Ōö“ó·“Ó¦ĖŁĀŹĒŅĘ½ŗāĻņÕż·“Ó¦ŅĘ¶Æ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ĪŖ£ŗŌö“óŃ¹Ēæ»ņÕߏĒŌö“óCO2ÅØ¶Č£¬
¹Ź“š°øĪŖ£ŗÉżøßĪĀ¶Č£»Ōö“óŃ¹Ē森
æ¼µć£ŗ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāĶ¼Ļ󔢷“Ó¦ĖŁĀŹ“óŠ”ÅŠ¶Ļ”¢Ķā½ēĢõ¼ž¶ŌĘ½ŗāµÄÓ°ĻģµČ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«Ź”µŚŅ»Ń§ĘŚĘŚÖÕæ¼ŹŌøßŅ»¼¶»ÆѧæĘŹŌ¾ķ¼×¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ĘĖćĢā
ÓĆ×ćĮæµÄNaOHĪüŹÕ448mLCl2(±ź×¼×“æö)ĀČĘų£¬¼ĘĖćÉś³ÉNaClµÄĪļÖŹµÄĮ攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«Ź”ÉīŪŚŹŠøßČżĮłŠ£4ŌĀĮŖæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
X”¢Y”¢Z”¢Q”¢MĪŖ³£¼ūµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£ÓŠ¹ŲŠÅĻ¢ČēĻĀ±ķ£ŗ
X | ¶ÆÖ²ĪļÉś³¤²»æÉȱɣµÄŌŖĖŲ£¬ŹĒµ°°×ÖŹµÄÖŲŅŖ³É·Ö |
Y | ×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµÄ3±¶ |
Z | ¶ĢÖÜĘŚÖŠ£¬ĘäŌ×Ó°ė¾¶×ī“ó |
Q | Éś»īÖŠ“óĮæŹ¹ÓĆĘäŗĻ½šÖĘĘ·£¬¹¤ŅµÉĻæÉÓƵē½āĘäŃõ»ÆĪļµÄ·½·ØÖʱø |
M | ŗ£Ė®ÖŠ“óĮæø»¼ÆµÄŌŖĖŲÖ®Ņ»£¬Ęä×īøßÕż»ÆŗĻ¼ŪÓėøŗ¼ŪµÄ“śŹżŗĶĪŖ6 |
ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ( )
A£®Ō×Ó°ė¾¶£ŗX > Y > M
B. ÓÉX”¢MŗĶĒāČżÖÖŌŖĖŲ²»æÉÄÜŠĪ³ÉĄė×Ó»ÆŗĻĪļ
C£®ĘųĢ¬Ēā»ÆĪļČČĪČ¶ØŠŌ£ŗM > Y > X
D£®Z”¢Q”¢MµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļæÉŅŌĮ½Į½·¢Éś·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«Ź”øßæ¼Ō¤²āĄķ×Ū»ÆѧŹŌ¾ķ¶ž£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø±¾Ģā16·Ö£©
£Ø1£©ĪŖĮĖ¼õĒįĘū³µĪ²ĘųŌģ³ÉµÄ“óĘųĪŪČ¾£¬ČĖĆĒæŖŹ¼Ģ½Ė÷ĄūÓĆNOŗĶCOŌŚŅ»¶ØĢõ¼žĻĀ×Ŗ»ÆĪŖĮ½ÖÖĪŽ¶¾ĘųĢåEŗĶFµÄ·½·Ø(ŅŃÖŖøĆ·“Ó¦”÷H<0). ŌŚ2 LĆܱÕČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæNOŗĶCO£¬µ±ĪĀ¶Č·Ö±šŌŚT1ŗĶT2Ź±£¬²āµĆø÷ĪļÖŹĘ½ŗāŹ±ĪļÖŹµÄĮæČēĻĀ±ķ£ŗ
T/”ę n/mol | NO | CO | E | F |
³õŹ¼ | 0.100 | 0.100 | 0 | 0 |
T1 | 0.020 | 0.020 | 0.080 | 0.040 |
T2 | 0.010 | 0.010 | 0.090 | 0.045 |
¢ŁĒė½įŗĻÉĻ±ķŹż¾Ż£¬Š“³öNOÓėCO·“Ó¦µÄ»Æѧ·½³ĢŹ½ .
¢Śøł¾Ż±ķÖŠŹż¾ŻÅŠ¶Ļ£¬ĪĀ¶ČT1ŗĶT2µÄ¹ŲĻµŹĒ(ĢīŠņŗÅ)__________”£
A£®T1>T2B£®T1<T2 C£®T1=T2 D£®ĪŽ·Ø±Č½Ļ
£Ø2£©ŅŃÖŖ£ŗ4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g); ¦¤H= - 1266.8 kJ/mol
N2(g) + O2(g) = 2NO(g) ; ¦¤H = + 180.5kJ/mol£¬
Ōņ°±“ß»ÆŃõ»ÆµÄČČ»Æѧ·½³ĢŹ½ĪŖ________________________________________”£
£Ø3£©500”ęĻĀ£¬ŌŚA”¢BĮ½øöČŻĘ÷ÖŠ¾ł·¢ÉśŗĻ³É°±µÄ·“Ó¦”£øō°å¢ń¹Ģ¶Ø²»¶Æ£¬»īČū¢ņæÉ×ŌÓÉŅĘ¶Æ”£
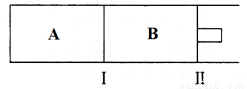
µ±ŗĻ³É°±ŌŚČŻĘ÷BÖŠ“ļĘ½ŗāŹ±£¬²āµĆĘäÖŠŗ¬ÓŠ1.0molN2£¬0.4molH2£¬0.4molNH3£¬“ĖŹ±ČŻ»żĪŖ2.0L”£Ōņ“ĖĢõ¼žĻĀµÄĘ½ŗā³£ŹżĪŖ___________£»±£³ÖĪĀ¶ČŗĶŃ¹Ēæ²»±ä£¬Ļņ“ĖČŻĘ÷ÖŠĶØČė0.36molN2£¬Ę½ŗā½«___________£ØĢī”°ÕżĻņ”±”¢”°ÄęĻņ”±»ņ”°²»”±£©ŅĘ¶Æ”£
£Ø4£©ŌŚĻąĶ¬µÄĆܱÕČŻĘ÷ÖŠ£¬ÓĆ·½·Ø¢ņŗĶ·½·Ø¢óÖʵƵÄĮ½ÖÖCu2O·Ö±š½ųŠŠ“߻ƷֽāĖ®µÄŹµŃé£ŗ
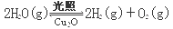 ¦¤H >0
¦¤H >0
Ė®ÕōĘųµÄÅØ¶Č£Ømol”¤L£1£©Ėꏱ¼ät (min)±ä»ÆČēĻĀ±ķ£ŗ
ŠņŗÅ | ĪĀ¶Č | 0 | 10 | 20 | 30 | 40 | 50 |
¢Ł | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
¢Ś | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
¢Ū | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
æÉŅŌÅŠ¶Ļ£ŗŹµŃé¢ŁµÄĒ°20 minµÄĘ½¾ł·“Ó¦ĖŁĀŹ ¦Ķ(O2)£½ £»“߻ƼĮµÄ“߻Ɗ§ĀŹ£ŗŹµŃé¢Ł ŹµŃé¢Ś£ØĢī”°>”±”¢”°<”±£©”£
£Ø5£©×īŠĀŃŠ¾æ·¢ĻÖ£¬ÓĆøōĤµē½ā·ØæÉŅŌ“¦ĄķøßÅضČŅŅČ©·ĻĖ®”£ŌĄķ£ŗŹ¹ÓƶčŠŌµē¼«ŗĶŅŅČ©-Na2SO4ČÜŅŗĪŖµē½āÖŹČÜŅŗ£¬ŅŅČ©·Ö±šŌŚŅõ”¢Ńō¼«×Ŗ»ÆĪŖŅŅ“¼ŗĶŅŅĖį”£
×Ü·“Ó¦ĪŖ:2CH3CHO+H2O CH3CH2OH+CH3COOH”£
CH3CH2OH+CH3COOHӣ
¹ż³ĢÖŠ£¬Į½¼«³ż·Ö±šÉś³ÉŅŅĖįŗĶŅŅ“¼Ķā£¬¾ł²śÉśĪŽÉ«ĘųĢ壬Ńō¼«µē¼«·“Ó¦·Ö±šĪŖ£ŗ
4OH£-4e£ØTO2”ü+2H2O£» ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«Ź”øßæ¼Ō¤²āĄķ×Ū»ÆѧŹŌ¾ķ¶ž£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄŹżÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®1L0.1mol”¤L-1µÄ°±Ė®ÖŠÓŠNAøöNH4+
B£®³£ĪĀ³£Ń¹ĻĀ£¬8gO2ŗ¬ÓŠ4NAøöµē×Ó
C£®±ź×¼×“æöĻĀ£¬22.4LČżĀČ¼×Ķéŗ¬ÓŠNAøö·Ö×Ó
D£®1molNa±»ĶźČ«Ńõ»ÆÉś³ÉNa2O2£¬Ź§Č„2NAµē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«Ź”½ĆÅŹŠø߶žµ÷ŃŠ²āŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚ25”ęµÄĢõ¼žĻĀ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®½«Ļ”°±Ė®ÖšµĪ¼ÓČėĻ”ĮņĖįÖŠ£¬µ±ČÜŅŗµÄpH=7Ź±£¬c(SO )= c(NH4£«)
)= c(NH4£«)
B£®pH=3µÄ“×ĖįČÜŅŗ£¬Ļ”ŹĶÖĮŌĢå»żµÄ10±¶ŗópH=4
C£®pH=11µÄNaOHČÜŅŗÓėpH£½3µÄ“×ĖįČÜŅŗµČĢå»ż»ģŗĻ£¬ČÜŅŗpH<7
D£®Ļņ0.1mol”¤L£1µÄ°±Ė®ÖŠ¼ÓČėÉŁĮæĮņĖįļ§¹ĢĢ壬ŌņČÜŅŗÖŠc(OH£) Ōö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«Ź”Ć·ÖŻŹŠøßŅ»ĻĀѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
(18·Ö)ŌŚµŚ3ÖÜĘŚÖŠ£¬ÖĆ»»ĖįÖŠĒāµÄÄÜĮ¦×īĒæµÄŌŖĖŲµÄŌŖĖŲ·ūŗÅĪŖ £¬»ÆѧŠŌÖŹ×īĪČ¶ØµÄŌŖĖŲ·ūŗÅŹĒ £¬×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌ×īĒæµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ £¬¼īŠŌ×īĒæµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ £¬ĻŌĮ½ŠŌµÄĒāŃõ»ÆĪļµÄ»ÆѧŹ½ŹĒ £¬øĆĮ½ŠŌĒāŃõ»ÆĪļÓėŃĪĖį”¢ĒāŃõÄĘČÜŅŗ·Ö±š·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”¢ £¬Ō×Ó°ė¾¶×ī“óµÄ½šŹōŌŖĖŲµÄĆū³ĘŹĒ £¬Ąė×Ó°ė¾¶×īŠ”µÄĄė×Ó½į¹¹Ź¾ŅāĶ¼ŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«Ź”½ŅŃōŹŠøßČż4ŌĀµŚ¶ž“ĪÄ£ÄāĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
£Ø16·Ö£©īŁ/Ģ¼øߊ§ĀĢÉ«“ß»ÆSuzuki ½»²ężĮŖ·“Ó¦ŹĒ½üÄźĄ“ÓŠ»śŗĻ³ÉµÄČȵćÖ®Ņ»£¬Čē·“Ó¦¢Ł£ŗ
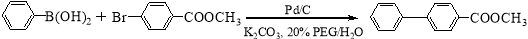
I II
»ÆŗĻĪļ¢ņæÉÓÉ»ÆŗĻĪļIIIŗĻ³É£ŗ

£Ø1£©»ÆŗĻĪļ¢ņµÄ·Ö×ÓŹ½ĪŖ £¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĆū³ĘĪŖ ”£
£Ø2£©»ÆŗĻĪļ¢ōµÄ½į¹¹¼ņŹ½ĪŖ ”£
£Ø3£©»ÆŗĻĪļ¢öÓėŠĀÖĘCu(OH)2Šü×ĒŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £Ø×¢Ć÷Ģõ¼ž£©”£
£Ø4£©»ÆŗĻĪļ¢õµÄŅ»ÖÖĶ¬·ÖŅģ¹¹Ģå¢ųÓöFeCl3ČÜŅŗĻŌ×ĻÉ«£¬ŗĖ“Ź²ÕńĒāĘ×·åĆ껿֮±ČĪŖ2£ŗ2£ŗ2£ŗ1£¬Ōņ»ÆŗĻĪļ¢ųµÄ½į¹¹¼ņŹ½ĪŖ _________ ”£Š“³ö»ÆŗĻĪļ¢ųÓė×ćĮæNaOHĖ®ČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £Ø×¢Ć÷Ģõ¼ž£©”£
£Ø5£©»ÆŗĻĪļ Óė»ÆŗĻĪļ
Óė»ÆŗĻĪļ ŌŚŅ»¶ØĢõ¼žæÉ·¢ÉśĄąĖĘ·“Ó¦¢ŁµÄ·“Ó¦£¬Ęä²śĪļµÄ½į¹¹¼ņŹ½ĪŖ ”£
ŌŚŅ»¶ØĢõ¼žæÉ·¢ÉśĄąĖĘ·“Ó¦¢ŁµÄ·“Ó¦£¬Ęä²śĪļµÄ½į¹¹¼ņŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¹ć¶«Ź”»ŻÖŻŹŠøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»Æѧ£ØĄķ£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŹÆÓĶŗĶĆŗ¶¼ŹĒÖŲŅŖµÄ»ÆŹÆÄÜŌ“£¬ĻĀĮŠÓŠ¹ŲŹÆÓĶŗĶĆŗµÄŠšŹöÕżČ·µÄŹĒ
A£®¶¼ŹĒ“æ¾»Īļ B£®¶¼ŗ¬ÓŠĢ¼ŌŖĖŲ C£®¶¼ŹĒæÉŌŁÉśÄÜŌ“ D£®¶¼ÓŠ¹Ģ¶ØµÄ·Šµć
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com