
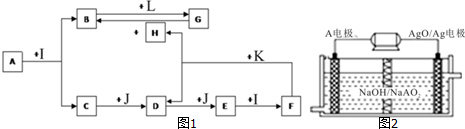
分析 F的浓溶液与常见固态非金属单质K加热可生成刺激性气体D和无色无味气体H.中学里符合该反应的只有碳跟浓硫酸或与浓硝酸反应,即K为碳,C与J连续反应得到E,E与液体I反应得到F,可推知J为O2,I为H2O,离子化合物A在水中发生水解反应得到B与C,B为白色胶状沉淀,L为氯碱工业中的常见产品,二者反应得到G,可推知B为Al(OH)3,L为NaOH、G为NaAlO2,则F为浓硫酸符合图中的物质间转化,C为H2S,D为SO2,E为SO3,H为CO2,A为一种Al与S组成的化合物,根据阳离子与阴离子的个数比为2:3,即可得知A为Al2S3,据此解答.
解答 解:F的浓溶液与常见固态非金属单质K加热可生成刺激性气体D和无色无味气体H.中学里符合该反应的只有碳跟浓硫酸或与浓硝酸反应,即K为碳,C与J连续反应得到E,E与液体I反应得到F,可推知J为O2,I为H2O,离子化合物A在水中发生水解反应得到B与C,B为白色胶状沉淀,L为氯碱工业中的常见产品,二者反应得到G,可推知B为Al(OH)3,L为NaOH、G为NaAlO2,则F为浓硫酸符合图中的物质间转化,C为H2S,D为SO2,E为SO3,H为CO2,A为一种Al与S组成的化合物,根据阳离子与阴离子的个数比为2:3,即可得知A为Al2S3,
(1)根据上面的分析可知,E为SO3,J为O2,
故答案为:SO3;O2;
(2)D为SO2,D通入足量稀Ba(NO3)2溶液反应的化学方程式为3SO2+3Ba(NO3)2+2H2O=3BaSO4↓+2NO+4HNO3,
故答案为:3SO2+3Ba(NO3)2+2H2O=3BaSO4↓+2NO+4HNO3;
(3)在铝制容器中加入食盐溶液,再将变黑的银器即表面为Ag2S浸入该溶液中,铝能还原出银,同是生成氢氧化铝和硫化氢,反应的方程式为2Al+3Ag2 S+3H2O=2Al(OH)3+6Ag+3H2S↑,
故答案为:2Al+3Ag2 S+3H2O=2Al(OH)3+6Ag+3H2S↑;
(4)A.根据电池总反应可知,该原电池的负极电极反应式为A-3e-+4OH-=AO2-+2H2O,正反应式为AgO+H2O+2e-=Ag+2OH-,所以该隔膜是阴离子交换膜,使氢氧根离子通过,故A错误;
B.根据电极反应AgO+H2O+2e-=Ag+2OH-,当电极上析出1.08 g即0.01mol Ag时,电路中转移的电子为0.02 mol,故B错误;
C.A电极的反应式为:A-3e-+4OH-=AO2-+2H2O,故C正确;
D.正极的电极反应式为:AgO+H2O+2e-=Ag+2OH-,故D错误,
故选C.
点评 本题考查无机物推断,该题突破口是:F的浓溶液与常见固态非金属单质K加热可生成刺激性气体D和无色无味气体H,再结合题目信息及转化关系推断,需要学生熟练掌握元素化合物性质,难度较大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| 浓度(c/mol•L-1) | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
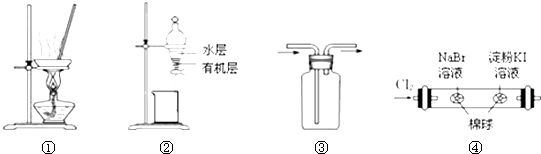
| A. | 用图①所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体 | |
| B. | 用图②所示装置,分离CCl4萃取碘水后的有机层和水层 | |
| C. | 按装置③所示的气流方向可用于收集H2、NH3等 | |
| D. | 用图④所示装置,可以证明氧化性:Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知室温下,某些弱酸的电离常数如下:
已知室温下,某些弱酸的电离常数如下:| CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | 1.7×10-5 | Ka1=4.2.×10-7 Ka2=5.6.×10-11 | 3×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
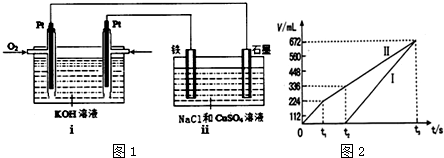
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 组成元素 | B、C | A、C | A、D | C、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com