
下列溶液中各粒子浓度关系不正确的是( )
A.由王水配成的稀溶液中:c(H+)=c(Cl-)+c(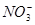 )
)
B.小苏打溶液中:c(Na+)=c(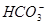 )+c(
)+c(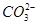 )+c(H2CO3)
)+c(H2CO3)
C.常温下,pH=7的(NH4)2SO4和NH3·H2O混合液中:c(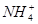 )=2c(
)=2c(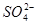 )
)
D.纯碱溶液中: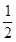 c(Na+)>c(
c(Na+)>c(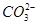 )>c(OH-)>c(
)>c(OH-)>c(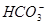 )
)
A
【解析】
试题分析:根据溶液中电荷守恒得:c(H+)=c(Cl-)+c(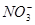 )+c(OH-),显然A错;因小苏打的化学式为NaHCO3,由Na、C元素守恒得:c(Na+)=c(
)+c(OH-),显然A错;因小苏打的化学式为NaHCO3,由Na、C元素守恒得:c(Na+)=c(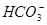 )+c(
)+c(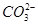 )+c(H2CO3),B正确;因在(NH4)2SO4和NH3·H2O的混合溶液中的电荷守恒得c(H+)+c(
)+c(H2CO3),B正确;因在(NH4)2SO4和NH3·H2O的混合溶液中的电荷守恒得c(H+)+c(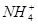 )=c(OH-)+2c(
)=c(OH-)+2c(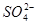 ),由于pH=7,溶液呈中性,故c(H+)=c(OH-),因此c(
),由于pH=7,溶液呈中性,故c(H+)=c(OH-),因此c(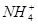 )=2c(
)=2c(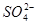 ),C正确;Na2CO3为强碱弱酸盐,在溶液中发生水解生成少量的
),C正确;Na2CO3为强碱弱酸盐,在溶液中发生水解生成少量的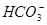 ,溶液呈碱性,
,溶液呈碱性,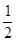 c(Na+)>c(
c(Na+)>c(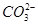 );
); 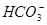 又水解生成H2CO3,使溶液中c(OH-)>c(
又水解生成H2CO3,使溶液中c(OH-)>c(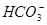 ),因此
),因此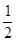 c(Na+)>c(
c(Na+)>c(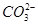 )>c(OH-)>c(
)>c(OH-)>c(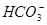 ),D正确,符合题意的为A。
),D正确,符合题意的为A。
考点:考查溶液中离子浓度关系的有关正误判断
点评:该题是中等难度的试题,也是高考中的常见题型。试题综合性强,侧重能力的培养。该题的关键是明确溶液中离子浓度之间应该遵循的几种守恒关系,即电荷守恒、物料守恒和质子守恒,并能结合题意灵活运用,有利于培养学生的逻辑思维能力和发散思维能力,提高学生分析问题、解决问题的能力。


科目:高中化学 来源: 题型:
 回答下列问题:
回答下列问题:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:浙江省滨江高中2008-2009学年高二五月综合测试化学试卷 题型:013
|
下列溶液中各粒子浓度关系不正确的是 | |
| [ ] | |
A. |
由王水配成的稀溶液中: |
B. |
小苏打溶液中: |
C. |
常温下,pH=7的(NH4)2SO4和NH3·H2O混合液中: |
D. |
纯碱溶液中: |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.由王水配成的稀溶液中:c(H+)=c(Cl-)+c(![]() )
)
B.小苏打溶液中:c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
C.常温下,pH=7的(NH4)2SO4和NH3·H2O混合液中:c(![]() )=2c(
)=2c(![]() )
)
D.纯碱溶液中:![]() c(Na+)>c(
c(Na+)>c(![]() )>c(OH-)>c(
)>c(OH-)>c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
A.由王水配成的稀溶液中:c(H+)=c(Cl-)+c(![]() )
)
B.小苏打溶液中:c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
C.常温下,pH=7的(NH4)2SO4和NH3·H2O混合液中:c(![]() )=2c(
)=2c(![]() )
)
D.纯碱溶液中:![]() c(Na+)>c(
c(Na+)>c(![]() )>c(OH-)>c(
)>c(OH-)>c(![]() )
)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com