
| A | B | C | D | E |
| ①能使溴水褪色 ②比例模型为  ③能与水在一定 条件下反应生 成物质C | ①由C、H两 种元素组成 ②球棍模型为  | ①由C、H、O三 种元素组成 ②能与Na反应, 但不能与NaOH 溶液反应 ③能与E反应生成 相对分子质量为 100的酯 | ①相对分子质量 比物质C小2 ②能由物质C氧 化而成 | ①由C、H、O三 种元素组成 ②球棍模型为  |
 .
. .
.分析 A使溴的四氯化碳溶液褪色,含有不饱和键,结合其比例模型可知,A为CH2=CH2,A能与水在一定条件下反应生成C,C由C、H、O三种元素组成,能与Na反应,但不能与NaOH溶液反应,故C为CH3CH2OH,根据B的组成元素及其球棍模型知,B是苯.结构简式为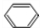 ;D由C氧化生成,相对分子质量比物质C小2,所以D是CH3CHO;E由C、H、O三种元素组成,由模型可知,E含有羧基和碳碳双键,可知E为CH2=CHCOOH,以此来解答.
;D由C氧化生成,相对分子质量比物质C小2,所以D是CH3CHO;E由C、H、O三种元素组成,由模型可知,E含有羧基和碳碳双键,可知E为CH2=CHCOOH,以此来解答.
解答 解:A使溴的四氯化碳溶液褪色,含有不饱和键,结合其比例模型可知,A为CH2=CH2,A能与水在一定条件下反应生成C,C由C、H、O三种元素组成,能与Na反应,但不能与NaOH溶液反应,故C为CH3CH2OH,根据B的组成元素及其球棍模型知,B是苯.结构简式为 ;D由C氧化生成,相对分子质量比物质C小2,所以D是CH3CHO;E由C、H、O三种元素组成,由模型可知,E含有羧基和碳碳双键,可知E为CH2=CHCOOH,
;D由C氧化生成,相对分子质量比物质C小2,所以D是CH3CHO;E由C、H、O三种元素组成,由模型可知,E含有羧基和碳碳双键,可知E为CH2=CHCOOH,
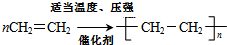
(1)A为CH2=CH2,与溴的四氯化碳溶液反应方程式为 ,生成物为1,2-二溴乙烷,乙烯发生加聚反应生成聚乙烯,反应方程式为:
,生成物为1,2-二溴乙烷,乙烯发生加聚反应生成聚乙烯,反应方程式为: ,
,
故答案为:1,2-二溴乙烷; ;
;
(2)A与氢气发生加成反应后生成物质F为乙烷,烷烃符合通式CnH2n+2,当烷烃中碳原子数目为4时开始出现同分异构体,故答案为:CnH2n+2;4;
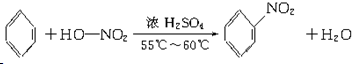
(3)B是苯,为无色具有特殊气味的液体,有毒,不溶于时,密度比水小,与氢气发生加成反应生成环己烷,与高锰酸钾不反应,结构简式为 ,与浓硝酸反应的化学方程式:
,与浓硝酸反应的化学方程式: ,
,
故答案为:②③; ;
;
(4)由C氧化生成D的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(5)C与E反应的反应方程式为CH2=CHCOOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH2=CHCOOCH2CH3+H2O,反应类型为取代反应,
故答案为:取代反应.
点评 本题考查有机物的推断,为高频考点,把握有机物的结构、官能团、性质为解答的关键,侧重分析与推断能力的考查,注意常见有机物的性质及转化,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 元素Y、W的简单阴离子具有相同的电子层结构 | |
| B. | 由X、W两种元素组成的化合物是离子化合物 | |
| C. | X的简单气态氢化物的热稳定性比W的强是因为X的氢化物分子间易形成氢键 | |
| D. | 离子半径:r(Z)<r(Y)<r(X)<r(W) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5% | B. | 9.1% | C. | 10.5% | D. | 15.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2 溶液中滴入过量NaOH溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向NaAlO2 溶液中通入过量的 CO2:CO2+2H2O+A1O2-═Al(OH)3↓+HCO3- | |
| C. | 0.01mol/L NH4Al(SO4)2 溶液与 0.02mol/L Ba(OH)2 溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| D. | 向Ca(ClO)2 溶液中通入过量的 SO2:C1O-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢件表面镀锌时,钢件与外电源的正极相连 | |
| B. | 由反应 (g)+H2(g)→ (g)+H2(g)→ (g)△H=+28.7kJ.mol-1,则环已二烯比苯稳定 (g)△H=+28.7kJ.mol-1,则环已二烯比苯稳定 | |
| C. | 常温时,pH=11的氨水与pH=3的盐酸等体积混合,所得溶液pH>7 | |
| D. | 合成氨反应N2+3H2?2NH3,当满足v(N2)逆:v(H2)逆:v(NH3)逆=1:3:2时,标志该反应已达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 试剂 | 方法 |
| A | 分离碘水中的碘 | 乙醇 | 萃取 |
| B | 分离乙酸乙酯和乙醇 | 氢氧化钠溶液 | 分液 |
| C | 除去乙醇中乙酸 | 氧化钙 | 蒸馏 |
| D | 除去乙烷中的乙烯 | 溴的四氯化碳溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤⑥ | B. | ①③④⑥ | C. | ②④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若温度不变,将容器的体积增大一倍,此时的SO2浓度变为原来的0.5倍 | |
| B. | 若平衡时SO2、O2的转化率相等,说明反应开始时,两者的物质的量这比为2:1 | |
| C. | 若从平衡体系中分离出SO3,则有利于提高SO2的转化率和加快正反应速率 | |
| D. | 平衡状态时SO2、O2、SO3的物质的量之比一定为2:1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com