
| 19.2g |
| 64g/mol |
| 3 |
| 8 |
| 0.3mol |
| n(H+) |
| 1.12L |
| 22.4L/mol |
| 0.3mol |
| 4 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | NaF | MgF2 | SiF4 |
| �۵�/K | 1266 | 1534 | 183 |
| C-O | C=O | C��O | |
| CO | 357.7 | 798.9 | 1071�� 9 |
| N-N | N=N | N��N | |
| N2 | 154.8 | 418.4 | 941.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
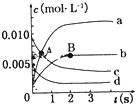 ��2L�ܱ������У�800��ʱ��Ӧ2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
��2L�ܱ������У�800��ʱ��Ӧ2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����| ʱ�䣨t�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
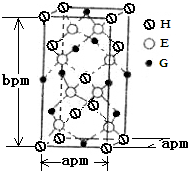 A��B��D��E��G��H����ǰ�����ڵ�Ԫ�أ�������ǰ�����ڵĻ�̬ԭ����A��δ�ɶԵ�����ࣻB��̬ԭ�ӵ�L���Ӳ��p�ܼ�����һ���չ����D �Ļ�̬ԭ�ӵ�2p�������1�����ӵ������������������ӵ����������෴��E�Ļ�̬ԭ��M����6���˶�״̬��ͬ�ĵ��ӣ� G�����ڱ���λ�ڵ�8�У�H��ԭ��������G��3��������Ϣ�ش��������⣺
A��B��D��E��G��H����ǰ�����ڵ�Ԫ�أ�������ǰ�����ڵĻ�̬ԭ����A��δ�ɶԵ�����ࣻB��̬ԭ�ӵ�L���Ӳ��p�ܼ�����һ���չ����D �Ļ�̬ԭ�ӵ�2p�������1�����ӵ������������������ӵ����������෴��E�Ļ�̬ԭ��M����6���˶�״̬��ͬ�ĵ��ӣ� G�����ڱ���λ�ڵ�8�У�H��ԭ��������G��3��������Ϣ�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Mx |
| VNA |
| A����������ܶȣ���g/LΪ��λ�� |
| B��VL���������������g��� |
| C��1mol��������������L��� |
| D��1L�������������ķ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com