
| A. | 配制银氨溶液:向氨水中加入过量的硝酸银溶液 | |
| B. | 银镜反应:向银氨溶液中滴加葡萄糖溶液后,热水浴 | |
| C. | 检验蔗糖的水解产物:先加碱中和,再滴入新制的氢氧化铜中加热 | |
| D. | 淀粉水解:向淀粉溶液中加入唾液,加热 |
分析 A.配制银氨溶液的方法:把氨水滴入硝酸银溶液,边振荡边逐滴加入至白色沉淀恰好溶解为止;
B.银氨溶液中滴加葡萄糖溶液后,应在水浴加热的条件下才能反应;
C.蔗糖水解生成葡萄糖,在碱性条件下可与新制的氢氧化铜加热反应;
D.淀粉在唾液淀粉酶的作用下水解生成葡萄糖.
解答 解:A.配制银氨溶液的方法:在洁净的试管中加入硝酸银溶液,边振荡边逐滴加入稀氨水,至最初产生的白色沉淀恰好溶解为止,制得银氨溶液,故A错误;
B.向银氨溶液中滴加葡萄糖溶液后,热水浴,可得到银镜,故B正确;
C.蔗糖水解生产葡萄糖,在碱性条件下可与新制的氢氧化铜加热反应,可观察到有砖红色沉淀生成,故C正确;
D.淀粉在唾液淀粉酶的作用下水解生成葡萄糖,最佳温度为37℃,故D正确.
故选A.
点评 本题考查化学实验方案的评价,侧重于物质的性质与检验的考查,综合考查学生化学知识的应用和实验评价能力,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
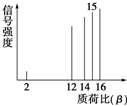 质谱法能够对有机分子进行结构分析.其方法是让极少量的(10-9 g)化合物通过质谱仪的离子化室,样品分子大量离子化,少量分子碎裂成更小的离子,然后测定其质荷比.其有机物样品的质荷比如图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),该有机物可能是( )
质谱法能够对有机分子进行结构分析.其方法是让极少量的(10-9 g)化合物通过质谱仪的离子化室,样品分子大量离子化,少量分子碎裂成更小的离子,然后测定其质荷比.其有机物样品的质荷比如图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),该有机物可能是( )| A. | 甲醇(CH3OH) | B. | 甲烷 | C. | 丙烷 | D. | 乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑦ | B. | ①③④⑥⑦ | C. | ①③⑥⑦ | D. | ①③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应的热化学方程式:N2(g)+3H2(g)═2NH3(l)△H=2(a-b-c) kJ•mol-1 | |
| B. | 该反应的热化学方程式:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)═NH3(g)△H=(a+b) kJ•mol-1 | |
| C. | 其他条件不变,升高温度,正、逆反应速率均增大,且H2的转化率增大 | |
| D. | T1>T2,且正反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 迄今人类发现的元素中,金属元素和非金属元素种数相近 | |
| B. | 元素周期表有18个纵行16个族,分为主族、副族、第Ⅷ族和零族 | |
| C. | 元素周期表有七个周期,分为短周期和长周期和不完全周期 | |
| D. | 人们在周期表中金属与非金属的分界处可以找到半导体材料,如硅、锗等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com