
【题目】下列离子方程式书写正确的是
A.用铜作电极电解硫酸铜溶液: 2Cu2+ + 2H2O ![]() 2Cu+ O2↑+4H+
2Cu+ O2↑+4H+
B.用银氨溶液检验乙醛中的醛基: CH3CHO+2Ag(NH3)2++2OH-![]() CH3COO-+NH4++3NH3+2Ag↓+H2O
CH3COO-+NH4++3NH3+2Ag↓+H2O
C.苯酚钠溶液中通入少量的CO2: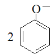 +H2O
+H2O![]()
![]() +CO32-
+CO32-
D.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e-= 4OH-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有机物G(1,4—环己二醇)是重要的医药中间体和新材料单体,可通过以下流程制备。

完成下列填空:
(1)写出A中官能团名称___。
(2)反应类型:反应①____;反应③____。
(3)写出B的结构简式___。
(4)一定条件下E脱氢反应得一种产物,化学性质比较稳定,易取代、难加成。该产物的结构简式为____。
(5)写出C→G的化学方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应N2+3H2![]() 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
A.3v正(N2)=v正(H2)B.v正(N2)=v逆(NH3)
C.v正(N2)=3v逆(H2)D.2v正(H2)=3v逆(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于价电子排布式为3s23p4的粒子的描述正确的是( )
A. 它的原子核外有三种形状不同的电子云
B. 它的原子核外电子共有16种不同的运动状态
C. 它可与H2反应生成常温时的液态化合物
D. 该原子的轨道表示式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于下列事实的解释错误的是( )
A.在蔗糖中加入浓硫酸后岀现发黑现象,说明浓硫酸具有吸水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C.氨溶于水的喷泉实验,说明氨气极易溶于水
D.向碘水中滴加CCl4,振荡静置分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表各组物质之间通过一步反应不可以实现如下图所示转化关系的是

选项 | X | Y | Z | 箭头上所标数字的反应条件 |
A | SiO2 | Na2SiO3 | H2SiO3 | ①与Na2CO3熔融 |
B | NaCl | NaHCO3 | Na2CO3 | ②加热 |
C | N2 | NO2 | HNO3 | ③加热 |
D | C | CO | CO2 | ④灼热炭粉 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种锂离子电池,在室温条件下可进行循环充放电,实现对磁性的可逆调控。一极为纳米Fe2O3,另一极为金属锂和石墨的复合材料,电解质只传导锂离子。电池总反应为:Fe2O3+6Li![]() 2Fe+3Li2O,关于此电池,下列说法不正确的是
2Fe+3Li2O,关于此电池,下列说法不正确的是
A.放电时,此电池逐渐靠近磁铁
B.放电时,正极反应为Fe2O3+6Li++6e-= 2Fe+3Li2O
C.放电时,正极质量减小,负极质量增加
D.充电时,阴极反应为Li++e-=Li
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢、氮、氧、硫,镁,铁、铜,锌等元素及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)某同学根据已学知识,推断Mg基态原子的核外电子排布为,
![]()
该同学所画的电子排布图违背了________________________________.
(2)Fe位于___________族_______区,Fe2+价电子排布式为_____________。
(3)MgCO3的分解温度____ BaCO3 (填“>” 或、“<”)
(4)C、N、O元素的第一电离能由大到小的顺序为_________________
(5)1mol[Cu(NH3)2]+中含有σ键的数目为___________
(6)下列有关说法不正确的是____。
A.热稳定性:NH3 >PH3,原因是NH3分子间存在氢键,而PH3分子间存在范德华力
B.SO2与CO2的化学性质有些类似,但空间结构与杂化方式不同
C.熔、沸点: SiF4< SiCl4< SiBr4 <SiI4 , 原因是分子中共价键键能逐渐增大
D.熔点: CaO > KCl > KBr,原因是晶格能逐渐减小
(7)晶体Cu的堆积方式如图所示,其中Cu原子在二维平面里放置时的配位数为_________,设Cu原子半径为a,晶体的空间利用率为______。(用含π,a、的式子表示,不必化简)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚磷酸二乙酯[HPO(OC2H5)2]是一种液态阻燃增塑剂。实验室采用PCl3和无水乙醇制备高纯度亚磷酸二乙酯,反应方程式为:PCl3 + 4C2H5OH → HPO(OC2H5)2 + HCl↑+2C2H5Cl + H2O;实验步骤如下:

①将45 mL CHCl3和46.00 g(1.0 mol)无水乙醇混合后加入250 mL三颈烧瓶中。
②从仪器A中滴加20 mL CHCl3和41.25 g (0.3 mol)PCl3混合溶液,用冰水控温6~8℃,开动搅拌器,约1 h滴加完毕。
③将反应物倒入烧杯中,用10%的Na2CO3溶液调节pH至7~8,再用去离子水洗涤三次,在仪器B中分离。
④减压蒸馏,收集产品,得29.60 g产品。
(1)装置图中仪器A为恒压滴液漏斗,其中支管的作用为______;倒置漏斗的作用为______;步骤③中仪器B名称为______。
(2)用碳酸钠溶液洗涤的目的是为了除去酸性物质______(填化学式)以及PCl3;
(3)从无水乙醇利用角度计算,本次实验产率为______(填数值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com