
A、
| ||
B、
| ||
| C、4x | ||
| D、8x |
| 2.8L |
| 22.4L/mol |
| 2.8L |
| 22.4L/mol |
| x |
| 4 |
| x |
| 4 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
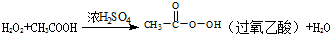
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用惰性电极电解饱和食盐水:2Cl-+2H+=H2↑+Cl2↑ |
| B、碱性氢氧燃料电池的正极反应式:O2+2H2O+4e-=4OH- |
| C、钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
| D、碳酸钠溶液呈碱性:CO32-+2H2O=H2CO3+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
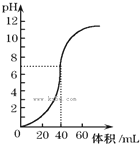 常温时,用1.0mol/L NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积关系如图所示.原硫酸溶液的物质的量浓度和完全反应后溶液的总体积是( )
常温时,用1.0mol/L NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积关系如图所示.原硫酸溶液的物质的量浓度和完全反应后溶液的总体积是( )| A、1 mol/L 60mL |
| B、0.5 mol/L 80mL |
| C、0.5 mol/L40mL |
| D、1 mol/L 80mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH溶液与NaOH溶液反应:CH3COOH+OH-=CH3COO-+H2O |
| B、硫氢化钠水解:HS-+H2O?H3O++S2- |
| C、NaHCO3溶液与NaOH溶液反应:HCO3-+OH-=CO2↑+H2O |
| D、FeCl3溶液与Na2S溶液反应:2Fe3++3S2-+6H2O=2Fe(OH)3↓+3H2S↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氮气的转化率增大 |
| B、氢气的转化率不变 |
| C、氨气在平衡混合气体中的含量一定增大 |
| D、氨气在平衡混合气体中的物质的量增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有以下6种物质,结合相关问题填空:
有以下6种物质,结合相关问题填空:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中导电粒子的数目增加,导电性增强 |
| B、醋酸的电离程度增大,[H+]减小 |
| C、再加入10mL pH=11 NaOH溶液,混合液pH=7 |
| D、溶液中由水电离出的[H+]=1×10-11mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com