
(本题共13分)焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一,为白色或黄色结晶粉末或小结晶,带有强烈的SO2气味,溶于水即生成NaHSO3。实验室可利用二氧化硫与亚硫酸钠反应制备焦亚硫酸钠。某研究小组进行如下实验:实验一:焦亚硫酸钠的制取
采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置II中有黄色晶体析出。
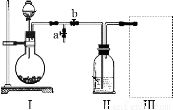
33.装置I中产生气体的化学方程式为 。
34.要从装置II中获得已析出的晶体,在实验室中需要使用到的玻璃仪器是: 。
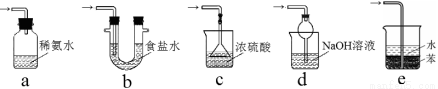
35.装置III用于处理尾气,防止污染环境。下列装置中,可选用的最合理装置(夹持仪器已略去)为 (填序号)。
实验二:焦亚硫酸钠的性质
36.将Na2S2O5溶于水配成溶液,
(1)欲证明所得溶液中的离子浓度大小关系:c(SO32—)>c(H2SO3),下列选项中可采用的实验方法是 。
a.测定溶液的pH
b.加入Ba(OH)2溶液
c.加入盐酸
d.加入品红溶液
e.用蓝色石蕊试纸检测
f.加入BaCl2溶液
(2)检验Na2S2O5晶体在空气中已被氧化的实验方案是 。
实验三:葡萄酒中抗氧化剂残留量的测定
37.葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不变”)。
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2014-2015学年陕西省渭南市高三教学质量检测(一模)化学试卷(解析版) 题型:填空题
(10分,三氧化二砷,俗称砒霜,分子式As2O3是最具商业价值的砷化合物及主要的砷化学开始物料。它也是最古老的毒物之一,无臭无味,外观为白色箱状粉末,故称砒霜。
(1)完成并配平下列化学方程式:
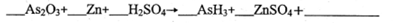
(2)As2O3在上述反应中显示出来的性质是_____________.
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.2molAsH3 ,则转移电子的物质的是为___________mol.
(4)砷化氢AsH3是一种很强的还原剂,在室温下它能在空气中自燃,其氧化产物是砒霸,写出该反应的化学方程式_________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省六校高三第二次联考理综化学试卷(解析版) 题型:选择题
用NA表示阿伏加徳罗常数的值,下列说法正确的是
A.常温常压下,2.24L 氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA
B.25℃时,2L0.1mol/L的Na2CO3溶液中含有的CO32-总数为0.2 NA
C.某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,生成SO3分子数为0.2 NA
D.30g乙酸和甲醛的混合物中氧原子数为NA
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列各项表达中正确的是
A.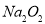 的电子式为
的电子式为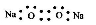
B.16g甲烷完全燃烧生成的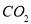 为11.2L(标准状况)
为11.2L(标准状况)
C.在氮原子中,质子数为7而中子数不一定为7
D.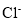 的结构示意图为
的结构示意图为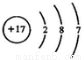
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.中子数为20的氯原子: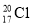
B.四氯化碳的电子式: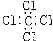
C.铝原子的结构示意图:
D.二氧化碳的结构式:O—C—O
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市奉贤区高三第二学期调研测试化学试卷(解析版) 题型:选择题
经测定某溶液中离子只有Na+、Ac—、H+、OH—四种,且离子浓度大小的排列顺序为:c(Ac—)>c(Na+)>c(H+)>c(OH—),则不可能的情形是
A.由pH=3的HAc与pH=11的NaOH溶液等体积混合而成
B.由0.2 mol/L HAc溶液与0.1 mol/L NaOH溶液等体积混合而成
C.由0.1 mol/L HAc溶液与等物质的量浓度等体积的NaOH溶液混合而成
D.向上述溶液中加入适量NaOH,可能使溶液中离子浓度大小改变为: c(Ac—) > c(Na+) > c(OH—) > c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市奉贤区高三第二学期调研测试化学试卷(解析版) 题型:选择题
下列有关Fe2(SO4)3溶液的叙述正确的是
A.该溶液中,K+、Fe2+、I—、Br—可以大量共存
B.用该溶液中溶解一定量铜粉,向所得溶液中再加入铁粉,若溶液中有Cu2+,则一定没有固体析出
C.将该溶液蒸干,得到的固体中混有氢氧化铁
D.100mL 0.1 mol/L该溶液和足量的Zn充分反应,生成1.12 gFe
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省西安地区八校高三下学期联考三理综化学试卷(解析版) 题型:填空题
(15分)将废旧锌锰电池处理得到含锰混合物,现以含锰混合物为原料制备锰锌铁氧体的主要流程如图l所示:
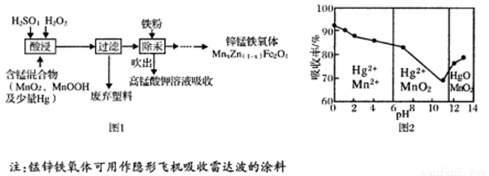
请回答下列问题:
(1)MnOOH中,锰元素的化合价为____。
(2)碱性锌锰干电池的电解质为KOH,Mn02参与的电板反应方程式为 。
(3)酸浸时,MnO2 与H2SO4、H2O2反应的离子方程式为 。
(4)在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如图2所示:
①pH对Hg吸收率的影响规律是 。
②在强酸性环境下Hg的吸收率高的原因可能是 。
(5)锰回收新方法:向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnOOH+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O
①当1molMnO2参加反应时,共有_____mol电子发生转移。
②MnOOH与浓盐酸在加热条件下也可发生反应,试写出其反应的化学方程式:_________________。
③已知:Ksp(MnCO3)=2.3×10-11、Ksp(Mn(OH)2))=2.1×10-13,欲制备MnCO3,选用的加料方式是______(填字母),原因是___________________________________。
a.将MnSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将MnSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有MnSO4溶液的反应容器中
d.以上三种方法都无法制得MnCO3
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二下学期期中考试化学试卷(解析版) 题型:选择题
最近,媒体报道不法商贩销售“致癌大米”,已验证这种大米中含有黄曲霉毒素(AFTB),其分子结构式为如图所示,人体的特殊基因在黄曲霉素的作用下会发生突变,有转变为肝癌的可能。一般条件下跟1mol AFTB起反应的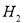 或NaOH的最大量分别是
或NaOH的最大量分别是
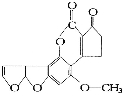
A.6mol;1mol B.5mol;1mol
C.6mol;2mol D.5mol;2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com