
����Ŀ�����á� Na��CO2����ؽ�CO2���Ϊ�����ҹ�������Ա���Ƴ��Ŀɳ�硰 Na��CO2����������Ʋ��Ͷ��̼����(MWCNT)Ϊ�缫�������ܷ�ӦΪ4Na��3CO2 ![]() 2Na2CO3��C���ŵ�ʱ�õ�ء����롱CO2���乤��ԭ����ͼ��ʾ��
2Na2CO3��C���ŵ�ʱ�õ�ء����롱CO2���乤��ԭ����ͼ��ʾ��

(1)�ŵ�ʱ�������ĵ缫��ӦʽΪ______________________________________________��
(2)�����ɵ�Na2CO3��Cȫ�������ڵ缫��������ת��0.2 mol e��ʱ��������������Ϊ________ g��
(3)ѡ�ø����������ĸʴ������������Һ���ŵ���___________________________________(����д����)��
���𰸡� 3CO2��4Na����4e��===2Na2CO3��C 15.8 �����Ժá�������Ʋ���Ӧ���ѻӷ���
��������(1)����CO2�õ��ӷ�����ԭ��Ӧ���ʵ缫����ʽΪ3CO2+4Na++4e-=2Na2CO3+C���ʴ�Ϊ��3CO2+4Na++4e-=2Na2CO3+C��
(2)���������ĵ缫��Ӧ3CO2+4Na++4e-=2Na2CO3+C
3 421
0.150.20.10.05��
m(��)=m(Na2CO3)+m(C)=106g/mol��0.1mol+12g/mol��0.05mol=11.2g��
���������ĵ缫��Ӧ4Na-4e-=4Na+
924
m(Na)0.2
m(Na)=4.6g����������������Ϊ11.2g+4.6g=15.8g���ʴ�Ϊ��15.8��
(3)ѡ���{������-�ĸʴ������������Һ���ŵ��ǵ����Ժã�������Ʋ���Ӧ���ѻӷ����ʴ�Ϊ�������Ժã�������Ʋ���Ӧ���ѻӷ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������NH3D+�У�����������������������֮��Ϊ��
A. 10��7��11 B. 11��11��8 C. 10��11��8 D. 11: 8:10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����I��������ͼװ�õ���Ʊ�LiOH�����缫�����Һ�ֱ�ΪLiOH��LiCl��Һ��
B�������ҺΪ__________��Һ���ѧʽ���������缫��ӦʽΪ_________________________��
��������Li+�� __________�缫Ǩ�ƣ��A����B������

(��)��ͼΪ��ɫ��Դ��������(CH3OCH3)ȼ�ϵ�����Ĺ���ԭ��ʾ��ͼ��b�缫��________����
��д�������ĵ缫��Ӧ����ʽ��__________________

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ�������
A. SiH4�ķе����CH4�����Ʋ�PH3�ķе����NH3
B. NH4��Ϊ��������ṹ�����Ʋ�PH4��ҲΪ��������ṹ
C. CO2�����Ƿ��Ӿ��壬���Ʋ�SiO2����Ҳ�Ƿ��Ӿ���
D. ���ʯ�ۻ�ʱ��Ҫ�ƻ����ۼ������Ʋ�C60�ۻ�ʱҲ�ƻ����۽�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaCl��NaBr��NaI��NaS��Һ����ѡ�õ��Լ���
A. ��ˮ B. AgNO3��Һ C. �� D. FeCl3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯������;�㷺��ij��������Ҫ�ɷ���NiFe2O4������������NiO��FeO��
CaO��SiO2�ȣ������ǴӸÿ����л���NiSO4�Ĺ���·�ߣ�
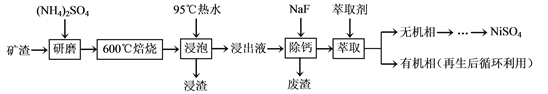
��֪��(NH4)2SO4��350�����ϻ�ֽ�����NH3��H2SO4��NiFe2O4�ڱ��չ���������
NiSO4��Fe2(SO4)3��
����Sn��λ�ڵ������ڵڢ�A�塣
��1������ǰ��������(NH4)2SO4�����ĥ�������ĥ��Ŀ����___________________��
��2�������ݡ�������Fe2(SO4)3����FeO(OH)�����ӷ���ʽΪ____________________��
���������ijɷֳ�Fe2O3��FeO(OH)�����________���ѧʽ����
��3��Ϊ��֤��Ʒ���ȣ�Ҫ��⡰����Һ������������ȡһ������Ľ���Һ���������ữ����SnCl2��Fe3+��ԭΪFe2+������SnCl2�����ʵ���������Fe3+���ʵ�����_______������ȥ������SnCl2����������K2Cr2O7����Һ�ζ���Һ�е�Fe2+����ԭ����ΪCr3+���ζ�ʱ��Ӧ�����ӷ���ʽΪ___________________��
��4��������Һ����c(Ca2+) = 1.0��10��3mol��L��1���������ʴﵽ99%ʱ����Һ��c(F��) = ________mol��L��1��[��֪Ksp (CaF2)=4.0��10��11]
��5���������У���ȡ������Һ������ȣ�V0/VA������Һ��Ni2+��Fe2+����ȡ��Ӱ������ͼ��ʾ��V0/VA�����ȡֵ��______��
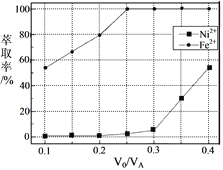
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������������ȷ����
A. �������ۼ�����Ϊ0.4NA�İ���(P4)�ͼ�������ʵ������
B. 10gŨ��Ϊ46�����Ҵ�ˮ��Һ�к��е���ԭ������Ϊ1.2NA
C. 2 g H2�ֱ���������C12��N2��ַ�Ӧ��ת�Ƶĵ�������Ϊ2NA
D. 1molFe(OH)3�뺬3molHI����Һ��ȫ��Ӧ����Һ������I-����ĿΪ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�Ľ������������������о���������Ҫ����;����ͼ�Ǵ����������Ʊ����Ĺ������̣�

��֪����1�����������Ҫ�ɷ���Al2O3�������������SiO2��Fe2O3�����ʣ�
��2����Һ�еĹ�������ƫ�����Ʒ�Ӧ�������ɹ������γ�������ѧ��Ӧ����ʽΪ2Na2SiO3+2NaAlO2+2H2O=Na2A12Si2O8��+4NaOH����ش��������⣺
��1����������Al2O3������������Һ��Ӧ�����ӷ���ʽΪ_________________________________��
��2���ڹ��������С��ữ��ʱ��������������B��________��������_______________________��д���ữ���̷�����Ӧ�Ļ�ѧ����ʽ��________________________________��
��3����ҵ����Al2O3��C��Cl2�ڸ��������·�Ӧ��ȡAlCl3��������ÿ����6.0 g̼���ʣ�ת��1 mol���ӣ���Ӧ�Ļ�ѧ����ʽΪ__________________________________��
��4��ijͬѧ�Ʋ������������������ȷ�Ӧ�õ����������л�����Fe2O3����������·�������֤��ȡһ���������Ͷ������ϡ�����У���Ӧһ��ʱ�����Ӧ��Ļ��Һ�еμ����ʼ���Һ���۲���Һ��ɫ�ı仯������֤�����������Ƿ���Fe2O3��
�����ʼ���_________(�ѧʽ)�����жϸ�ͬѧ��Ƶ�ʵ�鷽���ĺ�����_________(�������������������ԭ����_______________________________________����������������д����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥ�����е�Ca2+��Mg2+��![]() ����ɳ���ɽ���������ˮ��Ȼ������������������
����ɳ���ɽ���������ˮ��Ȼ������������������
������ ���ӹ���NaOH��Һ ��������HCl ���ӹ���Na2CO3��Һ ���ӹ���BaCl2��Һ
ͨ���̲��С����ε��ᴿ�����������ĸ�ʵ��ش��������⣺
(1)�����岽�����У������е���________��
(2)ʵ���ҽ���NaCl��Һ������ʱ��һ�������²������̣�
���̶���Ȧλ�� �����þƾ��� ������������(��������ʢ��NaCl��Һ) �����Ƚ���
��ֹͣ����
��ȷ�IJ���˳��Ϊ________��
(3)�ڴ��ξ���һϵ�в��������Һ�еμӹ�������Na2CO3��Һ�������ⲽ������Ŀ����______________________���ж�Na2CO3��Һ�Ѿ������ķ�����__________________��
(4)ʵ�����ォ�����Ƴɾ��εĹ����У����ܽ⡢���ˡ�������������IJ����ж�Ҫ�õ����������ֱ�˵���������������ʹ�ò�������Ŀ�ģ�
�ܽ�ʱ��______________________________________________________________��
����ʱ��______________________________________________________________��
����ʱ��______________________________________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com