
| A. | CO中混有CO2(NaOH溶液) | B. | H2中混有HCl(NaOH溶液) | ||
| C. | NO中混有NO2(水) | D. | CO2中混有HCl(饱和Na2CO3溶液) |
分析 A.二氧化碳与NaOH溶液反应,而CO不能;
B.HCl与NaOH溶液反应,而氢气不能;
C.二氧化氮与水反应生成NO;
D.二者均与碳酸钠溶液反应.
解答 解:A.二氧化碳与NaOH溶液反应,而CO不能,则利用NaOH溶液、洗气可除杂,故A正确;
B.HCl与NaOH溶液反应,而氢气不能,则利用NaOH溶液、洗气可除杂,故B正确;
C.二氧化氮与水反应生成NO,则利用水、洗气可除杂,故;
D.二者均与碳酸钠溶液反应,不能除杂,应选饱和NaHCO3、洗气,故D错误;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应为解答的关键,侧重分析与应用能力的考查,注意除杂试剂的选择,题目难度不大.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取3.25g NaCl | |
| B. | 用酸式滴定管量取20.00mL KMnO4溶液 | |
| C. | 用量筒量取10.51 mL盐酸 | |
| D. | 用容量瓶配制216mL 0.1mol/L NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | ①滴加稀HNO3 ②滴加BaCl2溶液 | 无明显现象 白色沉淀 | 原溶液一定含Ag+ |
| B | 滴加稀盐酸 | 有大量气泡产生 | 原溶液一定含CO32- |
| C | ①滴加稀HCl ②滴加AgNO3溶液 | 无明显现象 白色沉淀 | 原溶液一定含Cl- |
| D | ①加KSCN溶液 ②滴加氯水 | 无明显现象 溶液呈红色 | 原溶液一定含Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
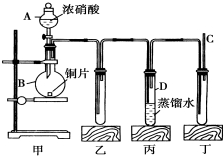 某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验.
某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中肼作还原剂 | |
| B. | 液态肼的燃烧热△H为-641.6kJ•mol-1 | |
| C. | 该动力源的突出优点之一是生成物对环境污染小 | |
| D. | 肼和过氧化氢反应的热化学方程式为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g);△H=-641.6kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片接电源的正极 | |
| B. | 铜片上发生的反应是:Ag++e-═Ag | |
| C. | 银片上发生的反应是:4OH--4e-═O2↑+2H2O | |
| D. | 需用硫酸铜溶液为电镀液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com