
| A£® | ·“Ó¦KClO3+6HClØT3C12”ü+KCl+3H2O£¬ĆæÉś³É1.5molC12×ŖŅʵē×ÓŹżĪŖ2.5NA | |
| B£® | ±ź×¼×“æöĻĀ£¬11.2LNOÓė11.2LO2»ģŗĻŗóĖłŗ¬·Ö×ÓŹżĪŖ0.75NA | |
| C£® | 1L0.1mol/LNH4ClČÜŅŗÖŠNH4+µÄŹżÄæĪŖ0.1NA | |
| D£® | 40gSiCÖŠŗ¬ÓŠSi-C¼üµÄŹżÄæĪŖ2NA |
·ÖĪö A£®·“Ó¦ÖŠKClO3+6HCl=KCl+3Cl2”ü+3H2OÖŠ£¬Ö»ÓŠClŌŖĖŲ»ÆŗĻ¼Ū·¢Éś±ä»Æ£¬ClŌŖĖŲ»ÆŗĻ¼Ū·Ö±šÓÉ+5¼Ū”¢-1¼Ū±ä»ÆĪŖ0¼Ū£¬¾Ż“Ė½ā“š£»
B.11.2LNOÓė11.2LO2»ģŗĻŗó·¢ÉśµÄ·“Ó¦ĪŖ2NO+O2ØT2NO2£¬2NO2?N2O4£¬Ōņ·“Ó¦ŗóµÄĘųĢåµÄĪļÖŹµÄĮæŠ”ÓŚ0£¬75mol£»
C£®°±øłĄė×ÓĪŖČõ¼īŃōĄė×Ó£¬Ė®ČÜŅŗÖŠ²æ·ÖĖ®½ā£»
D£®·ÖĪö½į¹¹£¬1mol SiCÖŠŗ¬ÓŠSi-C¼ü4mol£®
½ā“š ½ā£ŗA£®·“Ó¦ÖŠKClO3+6HCl=KCl+3Cl2”ü+3H2OÖŠ£¬Ö»ÓŠClŌŖĖŲ»ÆŗĻ¼Ū·¢Éś±ä»Æ£¬ClŌŖĖŲ»ÆŗĻ¼Ū·Ö±šÓÉ+5¼Ū”¢-1¼Ū±ä»ÆĪŖ0¼Ū£¬µ±ÓŠ3mol Cl2Éś³ÉŹ±£¬×ŖŅĘ5molµē×Ó£¬ŌņÉś³É1.5molĀČĘų×ŖŅĘ2.5molµē×Ó£¬¹ŹAÕżČ·£»
B.11.2LNOÓė11.2LO2»ģŗĻŗó·¢ÉśµÄ·“Ó¦ĪŖ2NO+O2ØT2NO2£¬2NO2?N2O4£¬Ōņ·“Ó¦ŗóµÄĘųĢåµÄĪļÖŹµÄĮæŠ”ÓŚ0£¬75mol£¬»ģŗĻŗóĖłŗ¬·Ö×ÓŹżÄæŠ”ÓŚ0.75NA£¬¹ŹB“ķĪó£»
C£®°±øłĄė×ÓĪŖČõ¼īŃōĄė×Ó£¬Ė®ČÜŅŗÖŠ²æ·ÖĖ®½ā£¬ĖłŅŌČÜŅŗÖŠNH4+µÄŹżÄæŠ”ÓŚ0.1NA£¬¹ŹC“ķĪó£»
D.40gSiCµÄĪļÖŹµÄĮæn=$\frac{40g}{40g/mol}$=1mol£¬¶ų1mol SiCÖŠŗ¬ÓŠSi-C¼ü4mol¼“4NAĢõ£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗA£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÓŠ¹Ų¼ĘĖć£¬ŹģĮ·ÕĘĪÕ¹«Ź½µÄŹ¹ÓĆŗĶĪļÖŹµÄ½į¹¹ŹĒ½āĢā¹Ų¼ü£¬×¢ŅāŃĪĄąĖ®½āµÄŠŌÖŹ£¬ÄŃ¶Č²»“ó£®


 ¼¤»īĖ¼Ī¬ÖĒÄÜѵĮ·æĪŹ±µ¼Ń§Į·ĻµĮŠ“š°ø
¼¤»īĖ¼Ī¬ÖĒÄÜѵĮ·æĪŹ±µ¼Ń§Į·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| n£ØSO32-£©£ŗn£ØHSO3-£© | 91£ŗ9 | 1£ŗ1 | 9£ŗ91 |
| pH | 8.2 | 7.2 | 6.2 |
| A£® | Na2SO3ČÜŅŗÖŠc£ØH+£©£¼c £ØOH-£© | |
| B£® | Na2SO3ČÜŅŗÖŠc£ØNa+£©£©£¾c £ØSO32-£©£¾c £ØHSO3-£©£¾c £ØOH-£©£¾c£ØH+£© | |
| C£® | µ±ĪüŹÕŅŗ³ŹÖŠŠŌŹ±£¬c£ØNa+£©£©£¾c £ØSO32-£©£¾c £ØHSO3-£©£¾c £ØOH-£©=c£ØH+£© | |
| D£® | µ±ĪüŹÕŅŗ³ŹÖŠŠŌŹ±£¬c£ØNa+£©£¾c £ØHSO3-£©+c £ØSO32-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 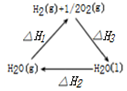 Ķ¼±ķŹ¾£ŗ”÷H1=”÷H2+”÷H3 | |
| B£® | 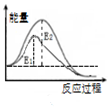 Ķ¼±ķŹ¾£ŗij·“Ó¦ŌŚ²»ÓĆÓėÓĆ“ß»Æ¼ĮŹ±£¬Ęä·“Ó¦»ī»ÆÄÜ·Ö±šŹĒE1ŗĶE2 | |
| C£® | 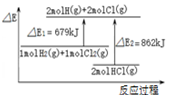 Ķ¼±ķŹ¾£ŗH2£Øg£©+Cl2£Øg£©=2HCl£Øg£©”÷H=-183kJ/mol | |
| D£® | 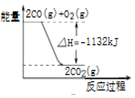 Ķ¼±ķŹ¾£ŗCOµÄČ¼ÉÕČČĪŖ1132KJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŃĪ | 0”ę | 10”ę | 20”ę | 30”ę | 40”ę | 50”ę | 60”ę | 100”ę |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -- | -- | -- | -- |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11£®l | 12.7 | 14.5 | 16.4 | -- |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³żČ„»ģŌŚCu·ŪÖŠµÄÉŁĮæMg·ŪŗĶAl·Ū£¬¼ÓĻ”ŃĪĖįŗó¹żĀĖ | |
| B£® | ·ÖĄėĘūÓĶŗĶĆŗÓĶ£¬æÉÓĆŻĶČ”µÄ·½·Ø | |
| C£® | ·ÖĄėĻõĖį¼ŲŗĶĀČ»ÆÄĘ¹ĢĢåµÄ»ģŗĻĪļ£¬æÉÓĆČܽā”¢¹żĀĖµÄ·½·Ø | |
| D£® | ½«ŃõĘųŗĶĒāĘųµÄ»ģŗĻĘųĢåĶعż×ĘČȵÄŃõ»ÆĶ£¬ŅŌ³żČ„ĘäÖŠµÄĒāĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH3CH2CH3 | B£® | CH3COOH | C£® | CH3COOCH3 | D£® | CH3OCH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
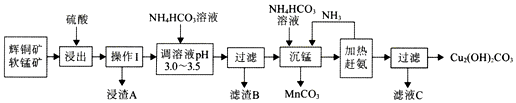
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
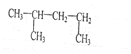
| A£® | ¢Ś¢Ż¢Ž | B£® | ¢Ś¢Ü | C£® | ¢Ü¢Ż | D£® | ¢Ł¢Ū¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com