
【题目】某铅氧化物(PbxOy),其中Pb有+2、+4两种化合物。研究小组测定其化学组成,实验流程如下:

测定过程涉及如下反应:I2+2Na2S2O3=2NaI+Na2S4O6
Pb2++EDTA4-=PbEDTA2-
⑴配制250mL1.6 molL-1的Na2S2O3溶液,需要的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管和_________________。
⑵过滤后,洗涤PbO2固体的操作为______________。
⑶“还原”过程中生成I2、CH3COOK、(CH3COO)2Pb,写出该反应的化学方程式______________;“I2的测定”中,应在滴入Na2S2O3溶液前,预先加入________________,以判断反应是否完全。
【答案】250mL容量瓶沿玻璃棒向过滤器中加蒸馏水至浸没滤渣,待液体自然流完后再重复操作2-3次2KI+PbO2+4CH3COOH = (CH3COO)2Pb+I2+2CH3COOK+2H2O淀粉
【解析】本题考查工艺流程,涉及一定物质的量浓度溶液的配制、实验基本操作等,(1)配制一定物质的量浓度的溶液,需要的仪器是:托盘天平(量筒) 、烧杯、玻璃棒、容量瓶、胶头滴管,本题缺少的实验仪器是容量瓶,因此填写250mL的容量;(2)洗涤沉淀:沿玻璃棒向过滤器中加蒸馏水至浸没滤渣,待液体自然流完后再重复操作2-3次;(3)根据流程图,有PbO2+KI+CH3COOH→I2+CH3COOK+(CH3COO)2Pb,PbO2中Pb的化合价由+4价→+2价,化合价降低2价,I-的化合价由-1价→0,化合价升高1价,最小公倍数为2,根据化合价升降法进行配平,以及原子守恒进行配平,PbO2+2KI+4CH3COOH→I2+2CH3COOK+(CH3COO)2Pb,生成物中缺少4个H、2个O,即生成物缺少2molH2O,方程式为:KI+PbO2+4CH3COOH = (CH3COO)2Pb+I2+2CH3COOK+2H2O,碘单质参与的反应I2+2Na2S2O3=2NaI+Na2S4O6,滴定时用淀粉作指示剂。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】下列有关实验正确的是( )
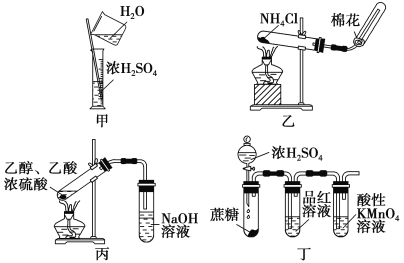
A.图甲:稀释浓硫酸
B.图乙:实验室制备氨气
C.图丙:实验室制备乙酸乙酯
D.图丁:检验浓硫酸与蔗糖反应产生的二氧化硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在碱性溶液中可发生如下反应:
2R(OH)3+3ClO-+4OH-=2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是
A.+3 B. +4 C. +5 D. +6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】课外活动小组探究久置的铝热剂(含Al、Al2O3、Fe2O3)的组成。称取样品3.510 g加入25.00 mL稀硫酸中,固体完全溶解,生成气体537.6 mL(标准状况),并得到溶液X。X不能使KSCN溶液变色。往X中加入过量NaOH溶液,沉淀经过滤、洗涤后,在空气中充分灼烧至恒重,冷却,称得剩余固体质量为2.400 g。下列说法一定正确的是
A. 样品中Al的物质的量为0.0160 mol
B. 样品中Al2O3的质量为0.408 g
C. 所用稀硫酸的浓度为2.64 mol·L-1
D. X中Fe2+与Al3+物质的量之比为15∶13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯原子对O3的分解有催化作用:
O3(g)+Cl(g)===ClO(g)+O2(g) ΔH1 ①
ClO(g)+O(g)===Cl(g)+O2(g) ΔH2 ②
该反应的能量变化如图所示,下列叙述中正确的是( )

A.反应O3(g)+O(g)===2O2(g)的ΔH=E1-E2
B.反应O3(g)+O(g)===2O2(g)的ΔH=E2-E3
C.反应O3(g)+O(g)===2O2(g)是吸热反应
D.反应O3(g)+O(g)===2O2(g)的ΔH=ΔH1+ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,第一种是含氧酸,第二种是强电解质,第三种是混合物的是
A.水、纯碱、空气 B. H2SO4、NaCl、烟
C. HNO3、盐酸、碱石灰 D.Fe2O3、BaSO4、饱和食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)在某温度下,将![]() 和
和![]() 各0.1mol的气态混合物充入10L的密闭容器中,充分反应,连续测定
各0.1mol的气态混合物充入10L的密闭容器中,充分反应,连续测定![]() 的变化,5S时测定
的变化,5S时测定![]() =0.0080mol/L并保护不变。
=0.0080mol/L并保护不变。
(1)反应在达到平衡过程中,![]() 的平均消耗速率为 mol/L·S;
的平均消耗速率为 mol/L·S;
(2)反应的平衡常数的表达式是![]() = ;
= ;
(3)此温度下,平衡常数值为 ;
(4)若在此温度下,在10L的密闭器充入0.2molHI气体,达到平衡时,HI的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(1)该反应的化学方程式为____。
(2)反应开始至2min,以气体X表示的平均反应速率为____。反应达限度时,Y的转化率为____,反应开始时与反应达平衡状态时的压强之比为____。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(X)=9 mol/(L·min),乙中v(Y)=0.1 mol/(L·s),则____中反应更快。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com