
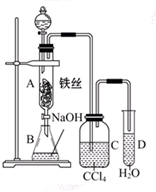
 某化学课外小组查阅资料知:苯和液溴在有铁存在的条件下可发生反应生 成溴苯和溴化氢,此反应为 放热反应.他们用如图所示 装置制取溴苯.已知:溴蒸气为红棕色
某化学课外小组查阅资料知:苯和液溴在有铁存在的条件下可发生反应生 成溴苯和溴化氢,此反应为 放热反应.他们用如图所示 装置制取溴苯.已知:溴蒸气为红棕色 ,观察到A中的现象反应混合液微沸,有红棕色气体充满A容器.实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是除去溶于溴苯中的溴,写出有关反应的化学方程式Br2+2NaOH═NaBr+NaBrO+H2O.
,观察到A中的现象反应混合液微沸,有红棕色气体充满A容器.实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是除去溶于溴苯中的溴,写出有关反应的化学方程式Br2+2NaOH═NaBr+NaBrO+H2O.分析 苯和液溴在铁作用下发生取代反应生成溴苯和溴化氢.由于反应放热,苯和溴两种反应物的沸点较低,所以,反应液沸腾,有红棕色溴蒸气挥发出来.溴单质可以与氢氧化钠溶液反应:Br2+2NaOH═NaBr+NaBrO+H2O,由此可知实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是除去溴苯中的溴.想证明苯和液溴发生的是取代反应,而不是加成反应,只需检验有无HBr生成,需检验溴离子和氢离子.可向试管D中加入AgNO3溶液,检验Br-,但溴易挥发,溴化氢气体中的溴蒸气对溴化氢的检验有干扰作用,因此,在检验溴化氢前必须先除去溴,C中盛放CCl4的作用除去溴,用紫色石蕊试液检验H+.
(1)苯与液溴在催化剂条件下发生取代反应生成溴苯;除去溴苯中的溴单质可用氢氧化钠洗涤;
(2)为证明苯和液溴发生的是取代反应,而不是加成反应,若为取代反应,只需检验有无HBr生成,需检验溴离子和氢离子,但溴易挥发,溴化氢气体中的溴蒸气对溴化氢的检验有干扰作用,因此需在检验溴化氢前必须先除去溴,检验氢离子用酸碱指示剂.
解答 解:(1)因溴与铁反应生成溴化铁:2Fe+3Br2 ═2FeBr3,苯和液溴在溴化铁的催化作用下生成溴苯和溴化氢,所以苯与液溴发生反应的化学方程式为: ;溴易挥发,苯与液溴反应放热,所以可以看到的现象为:反应液微沸,有红棕色气体充满A容器;溴化铁与氢氧化钠反应生成氢氧化铁沉淀,生成的溴苯中含有溴单质,溴单质可与氢氧化钠反应,反应的方程式为:Br2+2NaOH=NaBr+NaBrO+H2O;实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是:除去溶于溴苯中的溴,
;溴易挥发,苯与液溴反应放热,所以可以看到的现象为:反应液微沸,有红棕色气体充满A容器;溴化铁与氢氧化钠反应生成氢氧化铁沉淀,生成的溴苯中含有溴单质,溴单质可与氢氧化钠反应,反应的方程式为:Br2+2NaOH=NaBr+NaBrO+H2O;实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是:除去溶于溴苯中的溴,
故答案为: ;反应液微沸,有红棕色气体充满A容器;除去溶于溴苯中的溴;Br2+2NaOH=NaBr+NaBrO+H2O;
;反应液微沸,有红棕色气体充满A容器;除去溶于溴苯中的溴;Br2+2NaOH=NaBr+NaBrO+H2O;
(2)为证明苯和液溴发生的是取代反应,而不是加成反应,若为取代反应, ,只需检验有无HBr生成,需检验溴离子和氢离子,但溴易挥发,溴化氢气体中的溴蒸气对溴化氢的检验有干扰作用,可以用四氯化碳除去溴化氢气体中的溴蒸气,C中盛放CCl4的作用除去溴,检验Br-,可向试管D中加入AgNO3溶液,若产生淡黄色AgBr沉淀,则能证明,检验氢离子,向试管D中加入紫色石蕊试液,酸能使紫色石蕊试液试液变红色,
,只需检验有无HBr生成,需检验溴离子和氢离子,但溴易挥发,溴化氢气体中的溴蒸气对溴化氢的检验有干扰作用,可以用四氯化碳除去溴化氢气体中的溴蒸气,C中盛放CCl4的作用除去溴,检验Br-,可向试管D中加入AgNO3溶液,若产生淡黄色AgBr沉淀,则能证明,检验氢离子,向试管D中加入紫色石蕊试液,酸能使紫色石蕊试液试液变红色,
故答案为:紫色石蕊试液;溶液变红色.
点评 本题考查了苯的结构和性质以及溴苯的制备,侧重考查学生分析问题解决问题的能力,掌握反应的原理、各物质的性质以及操作的方法是解题的关键,题目难度中等.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题

| A. | a和b不连接时,铁片上会有金属铜析出且有电流产生 | |
| B. | a和b用导线连接时,Cu2+向铁电极移动 | |
| C. | a和b分别连接直流电源正、负极时,铁被保护,称为牺牲阳极的阴极保护法 | |
| D. | 无论a和b是否用导线连接,加入K3[Fe(CN)6]溶液有蓝色沉淀且溶液的温度都会升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2SO2(g)+O2(g)?2SO3(g)△H=-196.6 kJ•mol-1 | |
| B. | 2SO2(g)+O2(g)?2SO3(g)△H=-98.3 kJ•mol-1 | |
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=+98.3 kJ•mol-1 | |
| D. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-196.6 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com