
| A、x=1 |
| B、2min内A的反应速率为0.3 mol?(L?min)-1 |
| C、B的转化率为40% |
| D、若混合气体的密度不变则表明该反应达到平衡状态 |
| ||
| △t |
| ||
| 2min |
| 3 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 0.4mol |
| 1mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜与热的浓H2SO4反应放出1 mol气体时转移的电子数为2NA |
| B、1mol冰中含有的氢键数目为NA |
| C、标准状况下,22.4 L CCl4含有的分子数为NA |
| D、1 mol羟基含有的电子数为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.6g铁与足量盐酸反应转移的电子数为0.3NA |
| B、20g重水(2H2O)中含有的中子数为10NA |
| C、0.05molC8H18分子中所含共价键数为1.5 NA |
| D、室温下,28.0g乙烯和丙烯中混合气体中含有的碳原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向AgCl 浊液中加入 KBr 溶液,沉淀变成淡黄色,则 Ksp(AgCl)<Ksp(AgBr) |
| B、NH4HCO3的分解反应能自发进行因为熵变△S>0来解释 |
| C、丁达尔效应是区别胶体与溶液的一种常用物理方法 |
| D、人体内淀粉、脂肪、蛋白质的水解都是由酶所催化的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
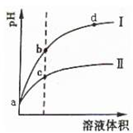 某温度下,将pH相同的盐酸和醋酸溶液分别稀释,平衡时溶液pH随溶液体积变化的曲线如图所示.据图判断下列叙述中,正确的是( )
某温度下,将pH相同的盐酸和醋酸溶液分别稀释,平衡时溶液pH随溶液体积变化的曲线如图所示.据图判断下列叙述中,正确的是( )| A、曲线Ⅰ为醋酸稀释时溶液pH变化曲线 |
| B、加入足量NaOH,b点溶液消耗的NaOH比c点溶液消耗的多 |
| C、a点时,加入少量相同大小的锌粒,与盐酸反应的速率大 |
| D、b点溶液中水的电离程度比c点溶液中水的电离程度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100 mL 1 mol?L-1的AlCl3溶液中,含有Al3+的数目为0.1NA |
| B、5.6 g Fe与足量的稀盐酸充分反应后,转移的电子数为0.3NA |
| C、标准状况下,22.4 L N2和O2的混合气体中,含原子数为NA |
| D、2.8 g乙烯与一氧化碳的混合气体中,含分子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com