
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有漂白性 |
| B | 将Cl2通入NaBr溶液中,然后加入CCl4,振荡、静置 | 比较氯与溴的氧化性强弱 |
| C | 将铜片分别与浓、稀硝酸反应 | 探究浓、稀硝酸氧化性的相对强弱 |
| D | 向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀。再加入少许浓硫酸,迅速搅拌。 | 探究浓硫酸的脱水性 |
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 高#考#资#源上图中的E和F构成量气装置,用来测定O2的体积。
高#考#资#源上图中的E和F构成量气装置,用来测定O2的体积。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

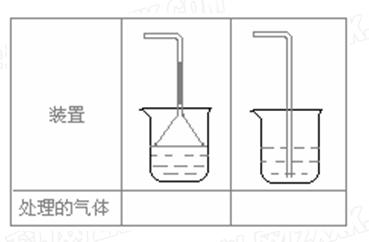
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
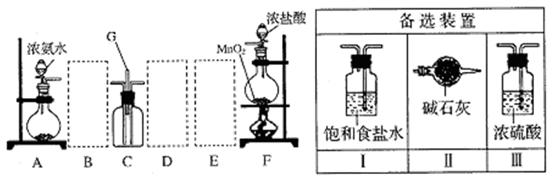
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 预期现象和结论 | |
| ① | 取少量上述漂白粉于试管中, | |
| ② | | |
| ③ | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
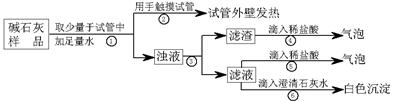
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| | 是否正确 | 简述理由 |
| 学生甲的观点 | | |
| 学生乙的观点 | | |
| 学生丙的观点 | | |
A. |
B. |
C. |
D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
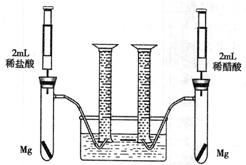
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com