
【题目】元素A的原子最外层有6个电子,元素B的原子最外层有3个电子,则A与B形成的化合物可能的化学式是
A.B2A3B.B2AC.BA2D.BA
科目:高中化学 来源: 题型:
【题目】工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)Si(g)+4HCl(g);△H=+Q kJmol﹣1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达平衡时,吸收热量为Q kJ
C.反应至4min时,若HCl浓度为0.24 mol/L,则H2的反应速率为0.03 mol/(Lmin)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100mL 1molL﹣1的NaOH溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如括号内为杂质,以下所用的除杂方法正确的是:
①氯气(HCl):气体通过饱和食盐水
②NaCl固体(I2):升华
③NaBr溶液(NaCl):加AgNO3溶液过滤
④溴水(I2):加苯萃取后分液
A.①②B.③④C.①②③D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M,N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )

A. 反应的化学方程式为:2MN B. t2时,正逆反应速率相等,达到平衡
C. t3时,正反应速率大于逆反应速率 D. t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W,X,Y,Z的原子序数依次增大,W,X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是( )
A.简单离子半径:W<X<Z
B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:W<Y
D.最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A.浓溶液一定是饱和溶液
B.析出晶体的溶液是饱和溶液
C.任何物质的饱和溶液,加热后都变成不饱和溶液
D.饱和溶液中,溶质的溶解速率大于结晶速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】参考如图,按要求回答下列问题: 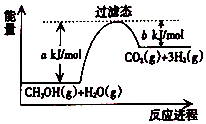
(1)甲醇质子交换膜燃料电池将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O反应生成CO2和H2 . 若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是(填“增大”、“减小”、“不变”),反应热△H的变化是(填“增大”、“减小”、“不变”).请写出CH3OH(g)和H2O(g)反应的热化学方程式 .
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的另一种反应原理是:
CH3OH(g)+ ![]() O2(g)CO2(g)+2H2(g)△H=﹣c kJ/mol
O2(g)CO2(g)+2H2(g)△H=﹣c kJ/mol
又知H2O(g)H2O(l)△H=﹣d kJ/mol.
则甲醇燃烧热的热化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com