
【题目】如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( ) 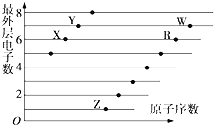
A.X和R在同一周期
B.原子半径:W>R>X
C.气态氢化物的稳定性:X>Y
D.X,Z形成的化合物中可能含有共价键
【答案】D
【解析】解:由图可知:原子序数X>Y>Z>R>W,再根据最外层电子数确定各元素所在族,都是短周期元素,可知X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,A.X为O元素、R为S元素,二者处于同一主族,故A错误;
B.同周期自左而右,原子半径减小,电子层越多原子半径越大,故原子半径S>Cl>O,故B错误;
C.同周期自左而右,金属性减弱,非金属性增强,气态氢化物越稳定,故气态氢化物的稳定性:HF>H2O,故C错误;
D.X、Z形成的化合物为氧化钠或过氧化钠,过氧化钠中过氧根离子中氧原子之间存在非极性共价键,故D正确.
故选D.
由图可知:原子序数X>Y>Z>R>W,再根据最外层电子数确定各元素所在族,都是短周期元素,可知X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,结合对应单质、化合物的结构和性质以及元素周期律知识解答该题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列物质所含分子数最多的是( )
A.0.8 mol二氧化碳
B.标准状况下2.24L氨气
C.3.6 g水
D.含NA个氢分子的氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素X、Y、Z、M、N的原子序数依次增大,X、Z和M分属于不同的周期,X、M元素可以形成负一价离子,Y原子的各能层电子数相同,Z原子最外层电子数是次外层的3倍,N元素原子的4p轨道上有3个未成对电子。
(1)五种元素中第一电离能最小的是________,电负性最大的是________。(填元素符号)
(2)Y元素原子的价层电子的电子排布图为________,该元素的名称是________。气态分子YM2的立体构型为________,YM2可形成多聚体(YM2)n的原因是________________。
(3)Z和N形成分子W的结构如图所示,化合物W的分子式为________,Z、N原子的杂化类型分别为________、________。

(4)已知化合物NX3是剧毒的气体,与AgNO3溶液反应有黑色Ag析出,同时生成W,此反应是检验微量NX3的方法,该反应的化学方程式是________________________________________________________________________。
(5)画出配离子YZ4X![]() 的结构式:________,1 mol该离子中含有的共价键数目为__________。
的结构式:________,1 mol该离子中含有的共价键数目为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化物是一类重要的化工原料,具有广泛的用途。完成下列填空:
(1)Na2S溶液中,水的电离程度会_________(填“增大”、 “减小”或“不变”);微热该溶液, pH 会_________(填“增大”、 “减小”或“不变”)。
(2)Na2S 溶液中各离子浓度由大到小的顺序为: ___________________________________。
(3)向 Na2S 和 Na2SO3 的混合溶液中加入足量的稀硫酸溶液,发生以下反应:
__ Na2S+ __ Na2SO3+__ H2SO4→__ Na2SO4+__ S↓+ __ H2O
①配平上述化学方程式,标出电子转移的方向和数目______。
②反应中被氧化的元素是______________。
(4)CuS和FeS都是难溶于水的固体,工业上可用 FeS 将废水中的 Cu2+转化为CuS除去,请结合相关原理进行解释:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某晶体的部分结构为正三棱柱(如图所示),这种晶体中A,B,C三种微粒数目之比为( ) 
A.3:9:4
B.1:4:2
C.2:9:4
D.3:8:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为镁-间二硝基苯电池的工作原理示意图。已知:电池放电时,铁转化为氢氧化镁,间二硝基苯则转化为间苯二胺。下列说法不正确的是
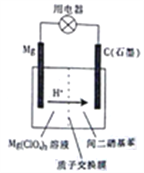
A. 电池放电时,电子由镁电极流出经过用电器流向石墨电极
B. 电池放电时,镁电极附近的电解质溶液的pH降低
C. 电池放电时,理论上每生成1mol间苯二胺就有12molH+通过质子交换膜
D. 电池放电时,石墨电板上发生的反应为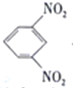 +12H+-12e-=
+12H+-12e-=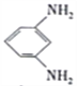 +4H2O
+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题.
(1)该实验反应物与生成物有机物的官能团种类有(填写名称).
(2)试管a中加入几块碎瓷片的目的是 .
(3)试管a中发生反应的化学方程式为 , 反应类型是 .
(4)反应开始前,试管b中盛放的溶液是 . 作用是 .
(5)反应结束后,振荡试管b,静置.反应结束后,试管b内的液体分成两层,乙酸乙酯在层(填写“上”或“下”).若分离10mL该液体混合物需要用到的主要玻璃仪器是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下元素周期表,以下说法正确的是
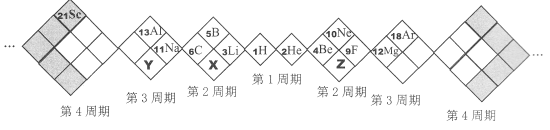
A. X、Y、Z元素分别为N、P、O
B. 所列元素都是主族元素
C. 原子半径:Z>X>Y
D. 稳定性:X的氢化物 < Y的氢化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com