
分析 (1)氯化镁溶液与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠;
(2)氯化铝与氢氧化钠反应,先生成沉淀,然后沉淀溶解,所以产生的沉淀为最大量时的一半,有两种情况,一种氢氧化钠不足,只沉淀一半铝离子,另一种情况铝离子全部被沉淀,剩余的氢氧化钠又溶解一半氢氧化铝沉淀,据此解答.
解答 解:(1)氯化镁溶液与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,离子方程式:Mg2++2OH-=Mg(OH)2↓,氢氧化镁为白色沉淀;
故答案为:产生白色沉淀;Mg2++2OH-=Mg(OH)2↓;
(2)氯化铝与氢氧化钠反应,先生成沉淀,然后沉淀溶解,所以产生的沉淀为最大量时的一半,有两种情况,一种氢氧化钠不足,只沉淀一半铝离子,发生反应方程式:AlCl3+3NaOH=Al(OH)3↓+3NaCl,消耗氢氧化钠物质的量为:$\frac{1}{2}$×0.1mol/L×0.01L×3=0.0015mol,体积为:$\frac{0.0015mol}{0.1mol/L}$=0.0015L,即15mL;
另一种情况,开始发生反应:AlCl3+3NaOH=Al(OH)3↓+3NaCl,AlCl3完全反应需要NaOH的物质的量=3n(AlCl3)=0.001mol×3=0.003mol,然后一半氢氧化铝沉淀溶解发生反应Al(OH)3+NaOH=NaAlO2+H2O,依据方程式消耗氢氧化钠物质的量为0.0015mol,共消耗氢氧化钠0.0045mol,体积为:$\frac{0.0045mol}{0.1mol/L}$=45mL;
故答案为:15或者45.
点评 本题考查了离子方程式的书写及有关计算,明确铝及其化合物之间转化是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
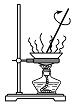 | 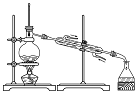 | 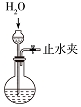 | 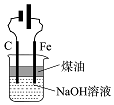 |
| A.蒸发氯化铝溶液的AlCl3 | B.分离乙酸钠和乙醇的混合液 | C.检查装置的气密性 | D.制备Fe(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 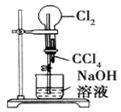 打开止水夹,挤压装置如图的胶头滴管使CCl4全部进入烧瓶 | |
| B. | 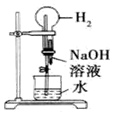 打开止水夹,挤压如图装置的胶头滴管使NaOH溶液全部进入烧瓶 | |
| C. | 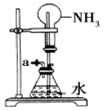 打开止水夹,用鼓气装置从如图装置的a处不断鼓入空气 | |
| D. |  打开止水夹,向如图装置的水槽中慢慢加入足量浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有强氧化性,可消毒杀菌,还原产物能吸附水中杂质 | |
| B. | 有强还原性,可消毒杀菌,氧化产物能吸附水中杂质 | |
| C. | 有强氧化性,能吸附水中杂质,还原产物能消毒杀菌 | |
| D. | 有强还原性,能吸附水中杂质,氧化产物能消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
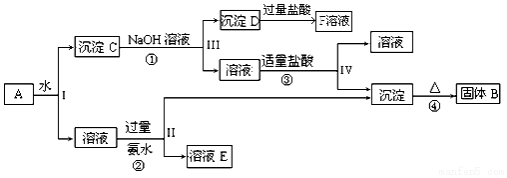
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散质微粒直径的大小关系:溶液>胶体>浊液 | |
| B. | 利用丁达尔效应可以区别溶液与胶体 | |
| C. | 胶体粒子比较小,可以通过半透膜 | |
| D. | 电泳现象可证明胶体属于电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
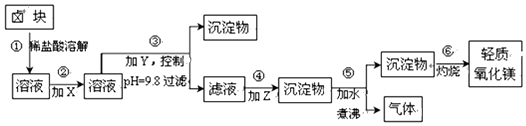
| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6 | b.双氧水(含30%H2O2) | 1500 |
| Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2200 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO) | 800 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
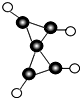 科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中黑圆代表碳原子,白圆代表氢原子,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中黑圆代表碳原子,白圆代表氢原子,下列说法中不正确的是( )| A. | 该分子的分子式C5H4 | |
| B. | 1mol该物质完全燃烧生成CO2与H2O时需耗6 mol O2 | |
| C. | 该物质完全燃烧生成的CO2与H2O的分子数比为5:4 | |
| D. | 1mol该物质完全燃烧生成CO2与H2O时转移电子数为24 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com