
某混合物A中含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下列所示的物质之间的转变[已知:NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3]:

据此判断:
(1)固体B所含物质的化学式为____________________________________________。
(2)固体E所含物质的化学式为_____________________________________________。
(3)反应①的离子方程式为________________________________________________。
(1)Al2O3 (2)(NH4)2SO4、K2SO4 (3)AlO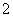 +CO2+2H2O===Al(OH)3↓+HCO
+CO2+2H2O===Al(OH)3↓+HCO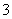
解析 铝及其化合物的性质与一般活泼金属元素的性质有差异之处,如Al2O3可溶于NaOH溶液,Fe2O3不能;KAl(SO4)2是一种复盐,可溶于水,完全电离,加入氨水可生成Al(OH)3沉淀,Al(OH)3在强碱溶液中溶解,而在氨水中不溶解。本题可用下列反应方程式描述从A开始的一系列变化:
Al3++3NH3·H2O===Al(OH)3↓+3NH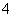 ,
,
2Al(OH)3△,Al2O3+3H2O,
Al2O3+2OH-===2AlO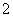 +H2O,
+H2O,
AlO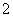 +CO2+2H2O===Al(OH)3↓+HCO
+CO2+2H2O===Al(OH)3↓+HCO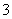 。
。


科目:高中化学 来源: 题型:
某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”,如图所示。在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗。为使液体顺利流下,还需插入“空气导入管”与大气相通。

(1)“空气导入管”下口应在________,上口应在________。
A.滤纸边沿下方 B.滤纸边沿上方
C.待过滤液面上方 D.待过滤液中
E.A和B项均可 F.C和D项均可
(2)试简要说明自动加液过滤的原理_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列陈述Ⅰ和Ⅱ正确并且有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2具有漂白性 | SO2可使溴水褪色 |
| B | SiO2具有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸具有强氧化性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+具有氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)现有34 g某气体,它的摩尔质量为17 g·mol-1。则:
①该气体的物质的量为________mol。②该气体所含分子数为________NA。
③该气体在标准状况下的体积为________L。
④该气体完全溶解于50mL水后稀释得2 L溶液,物质的量浓度___mol·L-1。
(2)将100 mL 0.5 mol·L-1 Na2CO3溶液加水稀释到1000 mL,稀释后
c(Na+)=____mol·L-1。
(3)______g H2O中的氧原子数目与标准状况下22.4 L CO2中的氧原子数目相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下在下列给定条件的溶液中,一定能大量共存的离子组是
A.中性溶液:Cu2+、Al3+、NO3-、SO42-
B.加入苯酚显紫色的溶液:K+、NH4+、Cl-、NO3-
C.加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42-
D.常温下,c(H+)/c(OH一)=1×10 12的溶液:K+、AlO2-、CO32-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
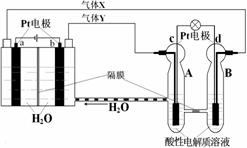
RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,RFC工作原理见图。下列有关说法正确的是
A.转移0.1mol电子时,a电极产生标准状况下O2 1.12L
B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
现有室温下的四种溶液,其pH如下表所示,下列有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | NaOH溶液 | 醋酸 | 盐酸 |
A.③④中分别加入适量醋酸钠晶体,两溶液pH均增大
B.②③两溶液等体积混合,所得溶液中:c(H+)>c(OH-)
C.分别加水稀释10倍,溶液的pH:①>②>④>③
D.V1L④和V2L①溶液混合后,若pH=7,则V1<V2
查看答案和解析>>
科目:高中化学 来源: 题型:
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反
应,其反应的产物有:HF、NO和HNO3 。则下列说法正确的是
A.反应过程中,被氧化与被还原的元素的物质的量之比为2:1
B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉
C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染
D.若反应中转移的电子数目为6.02×1023,生成22.4L NO气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com