
下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C—O是极性键 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
A
解析试题分析:A.原子半径N>O。但是由于氮原子2p能级半充满的稳定状态,失去电子较难,所以氮原子的第一电离能大于氧原子。正确。B. 在CO2分子中C=O是不同种元素的原子形成的共价键,是极性键。但是由于这两个C=O的键角为180°,是对称的,所以CO2为直线形分子。错误。C. 金刚石和石墨但是原子晶体,由于石墨是层状结构,在每一层内的共价键比金刚石的共价键结合力强,断裂难,所以石墨的熔点比金刚石的高。错误。D. HF的沸点高于HCl 是因为在HF的分子之间存在氢键,而HCl的分子之间只存在分子间作用力。由于氢键比分子间作用力大的多。所以HF的沸点高于HCl。错误。
考点:考查化学事实与原因的关系的知识。


科目:高中化学 来源: 题型:单选题
下列有关化学键与晶体结构说法正确的是
| A.两种元素组成的分子中一定只有极性键 |
| B.离子化合物的熔点一定比共价化合物的高 |
| C.非金属元素组成的化合物一定是共价化合物 |
| D.含有阴离子的化合物一定含有阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各项比较中前者高于(或大于或强于)后者的是
| A.CCl4和SiCl4的熔点 |
B.邻羟基苯甲醛(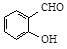 )和对羟基苯甲醛( )和对羟基苯甲醛(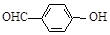 )的沸点 )的沸点 |
| C.SO2和CO2在水中的溶解度 |
| D.H2SO3和H2SO4的酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组物质,化学键类型相同、晶体类型相同且熔化时破坏作用力类型也相同的 ( )
| A.HCl KCl | B.CO2 SiO2 | C.NH4Cl CCl4 | D.NaOH Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲烷分子(CH4)失去一个H+,形成甲基阴离子(CH3-),在这个过程中,下列描述不合理的是( )
| A.碳原子的杂化类型发生了改变 |
| B.微粒的形状发生了改变 |
| C.微粒的稳定性发生了改变 |
| D.微粒中的键角发生了改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于化学键的叙述中,正确的是
| A.离子化合物可能含共价键 | B.共价化合物可能含离子键 |
| C.离子化合物中只含离子键 | D.离子化合物中一定含有金属离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com