
| A. | 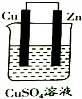 | B. | 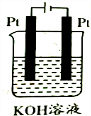 | C. | 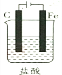 | D. | 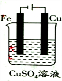 |
分析 A、没有外接电源的属于原电池,负极为锌失电子生成锌离子进入溶液,正极上铜离子放电析出铜单质;
B、有外接电源的属于电解池,阳极上氢氧根离子放电,阴极上氢离子放电,据此分析;
C、有外接电源的属于电解池,阳极上氯离子放电,阴极上氢离子放电,据此分析;
D、有外接电源的属于电解池,又属于电镀池,阳极上铜失电子,阴极上铜离子得电子,据此分析.
解答 解:A、没有外接电源的属于原电池,负极为锌失电子生成锌离子进入溶液,正极上铜离子放电析出铜单质,导致电解质溶液发生变化,故A错误;
B、有外接电源的属于电解池,阳极上氢氧根离子放电,阴极上氢离子放电,实际上是电解水导致溶液中溶液的体积减小,溶质的物质的量不变,则浓度增大,故B错误;
C、有外接电源的属于电解池,阳极上氯离子放电,阴极上氢离子放电,实际上是电解HCl,所以溶液中溶质的物质的量减小,浓度也减小,故C错误;
D、有外接电源的属于电解池,又属于电镀池,阳极上铜失电子,阴极上铜离子得电子,所以溶液中溶质的物质的量不变,浓度也不变,故D正确;
故选D.
点评 本题考查了原电池和电解池原理,明确离子放电顺序是解本题关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 原子序数:A>B>D>C | B. | 金属性B>D,非金属性A>C | ||
| C. | 原子半径:D>B>C>A | D. | 简单离子半径:C>B>D>A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2009年11月,中国政府公布了温室气体减排的行动目标,减排气体是的指二氧化硫 | |
| B. | 氮氧化物排放会引起光化学污染而与酸雨无关 | |
| C. | 开发新能源、燃煤脱硫、安装汽车尾气转化器等措施可以减少酸雨 | |
| D. | 二氧化碳是无毒的气体,可以任意排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 1 | 2 | 3 | 4 |
| 模型示意图 |  |  |  |  |
| A. | 模型1对应的物质的二氯代物有2种 | |
| B. | 模型2对应的物质的官能团是羧基 | |
| C. | 模型2对应的物质可与模型3对应的物质发生酯化反应 | |
| D. | 模型4对应的物质可以与氯气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2017届河南省南阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
根据下图海水综合利用的工业流程图,判断下列说法正确的是

已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
C.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
D.在过程④、⑥反应中每氧化0.2molBr-需消耗2.24LCl2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省长春市高二上学期期初考试化学试卷 题型:填空题
某二元酸(化学式用H2A表示)在水中的电离方程式是H2A===H++HA-,HA-?H++A2-。回答下列问题:
(1)Na2A溶液显(填“酸性”、“中性”或“碱性”),理由是(用离子方程式或必要的文字说明)。
(2)常温下,已知0.1mol·L-1NaHA溶液pH=2,则0.1mol·L-1H2A溶液中氢离子的物质的量浓度可能0.11mol·L-1(填“大于”、“等于”或“小于”),理由是。
(3)0.1mol·L-1N aHA溶液中各种离子浓度由大到小的顺序是。
aHA溶液中各种离子浓度由大到小的顺序是。
(4)Na2A溶液中,下列表述正确的是。
A.cNa++cH+=cHA-+2cA2-+cOH—
B.cNa+=2(cHA-+cA2-+cH2A)
C.cOH—=cHA-+cH++2cH2A
D.cOH—=cHA-+cH+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com