
| A. | KCl、HCl、S | B. | 金刚石、Na3PO4、MgO | ||
| C. | HF、SiC、Ar | D. | H2O、SiO2、K2CO3 |
科目:高中化学 来源: 题型:选择题
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 全氟丙烷的结构式为 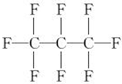 | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 全氟丙烷分子中只有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2和NH3的质量分数相等 | |
| B. | N2、H2、NH3的浓度之比为1:3:2 | |
| C. | 当断开1mol氮氮三键的同时,断开3mol氢氢键 | |
| D. | 氮气的体积分数保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种元素的最高正化合价中,Z的最大 | |
| B. | W晶体中只存在有共价键 | |
| C. | 原子半径:X>Y>Z | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
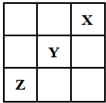 短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )| A. | Y的氢化物稳定性大于Z的氢化物稳定性 | |
| B. | Z一定是活泼的金属元素 | |
| C. | Y的最高价氧化物的水化物是一种强酸 | |
| D. | 1molX的单质可以跟足量水反应,转移的电子为2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt的中子数相同,互称为同位素 | |
| B. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt的质子数相同,互称为同位素 | |
| C. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt不能互称为同位素 | |
| D. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt是同一种核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,33.6 L SO3分子含有的硫原子数为1.5NA | |
| B. | 1 mol/L KI溶液中I-数目为NA | |
| C. | 0.1 mol Na+离子中所含的电子数为3.4 NA | |
| D. | 56g铁与足量的Cl2或S反应时转移电子数均为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com