

���� ����װ��ͼ��֪������ʵ���ԭ��Ϊ��Aװ�ò�����������Bװ�ø��ͨ��Cװ��������ͭ�ڼ��������·���������ԭ��Ӧ����ˮ��ˮ�ü�ʯ�����գ���������ͭ�������ı仯�ͼ�ʯ�ҵ������仯��ȷ����Ԫ�غ���Ԫ�ص������ȣ��ݴ��Ʋ�ˮ����ɣ�
��1��Ũ��������ˮ�ų��������ȣ���Ũ������ܶȴ���ˮ���ݴ˷�����
��2�����������л��п����ᱬը�����Լ���C������֮ǰ�����ž�װ���еĿ�����β����Ҫ�ɷ����������Ӱ�ȫ�Ƕȿ��ǣ����Խ������ռ��������ȼ��
��� �⣺����װ��ͼ��֪������ʵ���ԭ��Ϊ��Aװ�ò�����������Bװ�ø��ͨ��Cװ��������ͭ�ڼ��������·���������ԭ��Ӧ����ˮ��ˮ�ü�ʯ�����գ���������ͭ�������ı仯�ͼ�ʯ�ҵ������仯��ȷ����Ԫ�غ���Ԫ�ص������ȣ��ݴ��Ʋ�ˮ����ɣ�
��1��Ũ��������ˮ�ų��������ȣ���Ũ������ܶȴ���ˮ��������Ũ������ע��ˮ���ܻ�������Һ�ٷж�����Σ�գ�ϡ��Ũ����IJ��������������ձ��з���������ˮ��Ȼ��Ũ���������ձ��ڱ���������ˮ�У�ͬʱ�ò����ò��������裬
�ʴ�Ϊ�����ܻ�������Һ�ٷж�����Σ�գ������ձ��з���������ˮ��Ȼ��Ũ���������ձ��ڱ���������ˮ�У�ͬʱ�ò����ò��������裻
��2�����������л��п����ᱬը�����Լ���C������֮ǰ����Aװ���м���ϡ�����п������Ӧһ��ʱ�����F���ռ�һС�Թ����壬��Ĵָ��ס�Թܿڣ������ƾ����Ϸ�����������������������۵�������˵��װ���������Ѿ�����������C�����ȣ�β����Ҫ�ɷ����������Ӱ�ȫ�Ƕȿ��ǣ����Խ������ռ���������F����ȼ��
�ʴ�Ϊ������Aװ���м���ϡ�����п������Ӧһ��ʱ�����F���ռ�һС�Թ����壬��Ĵָ��ס�Թܿڣ������ƾ����Ϸ�����������������������۵�������˵��װ���������Ѿ������������ռ���������F����ȼ��
���� ������Ҫ����ʵ�����������ʵ��ԭ���ķ�������һ�����ۺ��ԣ��ܹ�����ѧ���������⡢����������������Ŀ�Ѷ��еȣ�


 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ũ�Ȳ��ٱ仯 | B�� | ������ѹǿ���ٸı� | ||
| C�� | ����ķ��������ٱ仯 | D�� | �������Ũ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 2��1 | C�� | 1��2 | D�� | 4��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������������������ѧУ�߶��ο�һ��ѧ���������棩 ���ͣ������
��1������ˮ��Һ�������ԣ���ԭ��Ϊ (�����ӷ���ʽ��ʾ����0��1 mol��L-1�İ�ˮ�м���������NH4Cl���壬��Һ��PH (����ߡ����͡�������������������������Һ�е�NH4+��Ũ�� (�����С������
��2������識��ȷֽ�ɵõ�N2O��H2O��250��ʱ����������ܱ������зֽ�ﵽƽ�⣬�÷ֽⷴӦ�Ļ�ѧ����ʽΪ ��ƽ�ⳣ������ʽΪ ������1mol�������ȫ�ֽ⣬ת�Ƶĵ�����Ϊ mol��
��3����N2O��NO��Ӧ����N2��NO2�������仯��ͼ��ʾ��������1molN2����H= kJ��mol-1��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������������������ѧУ�߶��ο�һ��ѧ���������棩 ���ͣ�ѡ����
��д��ڿ�ȼ��(CH4•nH2O���壩����֪��CH4•nH2O(s�� 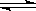 CH4(g��+nH2O(l����Q(Q��0������ܹ����ڿ�ȼ��������Ϊ��������������е�( ��
CH4(g��+nH2O(l����Q(Q��0������ܹ����ڿ�ȼ��������Ϊ��������������е�( ��
A�����¸�ѹ B�����µ�ѹ C�����µ�ѹ D�����¸�ѹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na3N | B�� | CH3COONa | C�� | NaOH | D�� | Na2O2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com