
【题目】工业上用发烟![]() ,把潮湿的
,把潮湿的![]() 氧化为棕色的烟
氧化为棕色的烟![]() 来除去
来除去![]() ,
,![]() 中部分氯元素转化为最低价态。下列说法不正确的是( )
中部分氯元素转化为最低价态。下列说法不正确的是( )
A.![]() 属于强酸,
属于强酸,![]() 中Cr元素显
中Cr元素显![]() 价
价
B.该反应除生成![]() 外,还生成了另一种强酸
外,还生成了另一种强酸
C.该反应中,参加反应的![]() 与
与![]() 物质的量之比为1∶2
物质的量之比为1∶2
D.作氧化剂的![]() 与参加反应的
与参加反应的![]() 物质的量之比为3∶16
物质的量之比为3∶16
【答案】D
【解析】
A.Cl元素非金属性较强,HClO4属于强酸;CrO2(ClO4)2中O为-2价、Cl为+7价,则Cr元素显+6价,故A正确;
B.Cl元素非金属性较强,HClO4属于强酸,生成盐酸,也属于强酸,故B正确;
C.该反应的离子方程式为:19ClO4-+8Cr3++4H2O=8CrO2(ClO4)2+3C1-+8H+,反应中参加反应的![]() 与
与![]() 物质的量之比为1∶2,故C正确;
物质的量之比为1∶2,故C正确;
D. 该反应的离子方程式为:19ClO4-+8Cr3++4H2O=8CrO2(ClO4)2+3C1-+8H+,ClO4-作氧化剂,发生变价的Cl原子为3mol,没有变价的Cl原子为16mol;Cr3+做还原剂,发生变化的Cr3+为8mol,所以![]() 与参加反应的
与参加反应的![]() 物质的量之比为3∶8,故D错误;
物质的量之比为3∶8,故D错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】结合已学知识,并根据下列一组物质的特点回答相关问题。
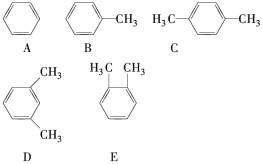
(1)邻二甲苯的结构简式为____(填编号,从A~E中选择)。
(2)A、B、C之间的关系为____(填序号)。
a.同位素 b.同系物 c.同分异构体 d. 同素异形体
(3)请设计一个简单实验来检验A与D,简述实验操作过程:_____________。
(4)有机物同分异构体的熔沸点高低规律是“结构越对称,熔沸点越低”,根据这条规律,判断C、D、E的熔沸点由高到低的顺序:______(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列有机物的类别及所含官能团的名称。
(1)CH3CH=CH2____、_________;
(2)HC≡C—CH2CH3__________、__________;
(3)![]() _________、___________;
_________、___________;
(4)![]() _________、_________;
_________、_________;
(5)![]() _________、___________;
_________、___________;
(6)CH3CH2—O—CH3__________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列说法错误的是( )
A.将6.4gSO2溶于水,溶液中H2SO3、HSO3-、SO32-的个数之和为0.1NA
B.![]() 和
和![]() 的混合物中所含阴离子
的混合物中所含阴离子![]() 总数为0.1NA
总数为0.1NA
C.19.2g铜完全溶于一定浓度的硝酸中,转移电子数一定为0.6NA
D.标准状况下,![]() 和
和![]() 的混合气体中所含氢原子数为3NA
的混合气体中所含氢原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某合作学习小组讨论辨析:
①氯化钠固体和氯化氢气体都不导电是因为二者中都不存在离子
②碳酸钠、氢氧化钡、氯化铵都属于离子化合物
③醋酸、烧碱和过氧化钠分别属于酸,碱和碱性氧化物
④氨气、水和硫酸钡分别属于非电解质、弱电解质和强电解质
⑤碳酸钠晶体在空气中风化是化学变化,硫酸铜溶液导电是化学变化
⑥用玻璃棒蘸取溶液进行焰色反应实验,火焰呈黄色说明溶液中含有![]()
⑦用![]() 溶液、品红试液都可以区分CO2和SO2这两种气体
溶液、品红试液都可以区分CO2和SO2这两种气体
上述说法正确的是( )
A.①④⑤⑥B.②④⑦C.①②③⑤D.②④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等浓度的NaOH溶液分别滴加到等pH、等体积的HA、HB两种弱酸溶液中,溶液的pH与粒子浓度比值的对数关系如图所示。下列叙述错误的是( )
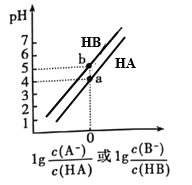
A. a点时,溶液中由水电离的c(OH-)约为1×10-10 mol·L-1
B. 电离平衡常数:Ka(HA)< Ka(HB)
C. b点时,c(B-)=c(HB)>c(Na+)>c(H+)>c(OH-)
D. 向HB溶液中滴加NaOH溶液至pH=7时:c(B-)> c(HB)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子电池的广泛应用要求处理锂电池废料以节约资源、保护环境。锂离子二次电池正极铝钴膜主要含有LiCoO2、A1等,处理该废料的一种工艺如下图所示:
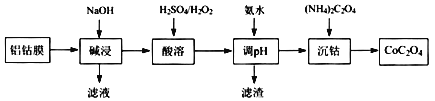
回答下列问题:
(l) Li元素在元素周期表中的位置为____________,LiCoO2中Co的化合价是____。
(2)“碱浸”时Al溶解的离子方程式为________。
(3)“酸溶”时加入H2O2的目的是____,调节pH后所得滤渣主要为____。
(4)“沉钴”的离子方程式为________。
(5)配制100 mL l.0 mol/L (NH4)2C2O4溶液,需要的玻璃仪器除玻璃棒、烧杯外,还需要_________。
(6)取CoC2O4固体4.41 g在空气中加热至300℃,得到钴的氧化物2.41 g,则该反应的化学方程式为 _________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.常温下pH为2的醋酸溶液中由H2O电离出的H+数为10-12NA
B.标准状况下,28gCO与22.4LSO3所含分子数都为NA
C.50mL8mol/L的浓盐酸与足量的MnO2加热反应,生成Cl2的分子数为0.1NA
D.在反应S+2KNO3+3C![]() K2S+N2↑+3CO2↑中,每生成2NA个气体分子,参加反应的氧化剂的物质的量为1.5mol
K2S+N2↑+3CO2↑中,每生成2NA个气体分子,参加反应的氧化剂的物质的量为1.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】思维辨析:
(1)乙醇易溶于水,是因为乙醇分子间存在氢键。________
(2)HO—CH2CH2—OH也可与Na反应,断裂C—O键。________
(3)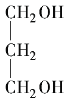 的命名是1,3二丙醇。________
的命名是1,3二丙醇。________
(4)1丙醇在氢氧化钠溶液中加热也可发生消去反应。________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com