
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.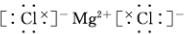 .
.分析 由元素在周期表中位置,可知①为C、②为N、③为F、④为Mg、⑤为Al、⑥为S、⑦为Cl、⑧为Ar、⑨为K、⑩为Br.
(1)稀有气体原子最外层为稳定结构,化学性质最不活泼;
(2)氢氧化铝是两性氢氧化物;铝与氢氧化钾反应生成偏铝酸钾与氢气;
(3)④元素与⑦元素形成的化合物为MgCl2,由镁离子与氯离子构成;
(4)高氯酸是最强的无机含氧酸.
解答 解:由元素在周期表中位置,可知①为C、②为N、③为F、④为Mg、⑤为Al、⑥为S、⑦为Cl、⑧为Ar、⑨为K、⑩为Br.
(1)由元素位置可知③为F元素,稀有气体Ar原子最外层为稳定结构,化学性质最不活泼,其原子核外电子数为18,原子结构示意图为: ,
,
故答案为:F; ;
;
(2)表中能形成两性氢氧化物的元素是Al,⑨最高价氧化物的水化物为KOH,铝与氢氧化钾反应生成偏铝酸钾与氢气,化学反应方程式为:2Al+2KOH+2H2O=2KAlO2+3H2↑,
故答案为:Al;2Al+2KOH+2H2O=2KAlO2+3H2↑;
(3)④元素与⑦元素形成的化合物为MgCl2,由镁离子与氯离子构成,其电子式为: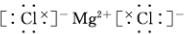 ,
,
故答案为: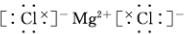 ;
;
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是:HClO4,
故答案为:HClO4.
点评 本题考查元素周期表与元素周期律综合应用,题目侧重对化学用语的考查,熟练掌握元素化合物知识,有利于基础知识的巩固.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1L1mol/L的NaCl溶液中取出500 ml,其浓度是0.5mol/L | |
| B. | 制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况) | |
| C. | 0.5L 2mol/LBaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 | |
| D. | 10g 98%硫酸(密度为1.84g/cm3)与1OmL 18.4mol/L硫酸的浓度是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只要有能量变化,则一定发生了化学反应 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 所有单质和化合物中,一定存在化学键 | |
| D. | 酸碱中和反应一定是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S在过量的O2中充分燃烧,可得SO3 | |
| B. | 除去在Na2CO3固体中混有的NaHCO3的最好办法是通入过量的CO2 | |
| C. | 鉴别NaHCO3溶液与Na2CO3溶液,可用澄清的石灰水 | |
| D. | 等物质的量的Na2CO3和NaHCO3与盐酸反应,消耗HCl的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY2一定能与水反应 | B. | X可能是ⅣA、VA或ⅥA族元素 | ||
| C. | 符合要求的XY2物质有两种 | D. | X、Y一定不是同一主族的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中性溶液:Fe3+、K+、Cl-、SO42- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-10的溶液:K+、Ba2+、NO3-、Cl- | |
| C. | 0.1mol/LNaAlO2溶液:H+、Na+、Cl-、SO42- | |
| D. | 与Al反应放出H2的溶液:Mg2+、Ca2+、HCO3-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com