
| A. | 甲烷的燃烧 | B. | 原子结合成分子 | ||
| C. | 分解反应 | D. | 灼热的碳与二氧化碳反应 |
分析 过程一定吸热能量说明该反应是吸热反应,当反应物的能量低于生成物总能量时,反应是吸热反应,吸热反应是化学反应中反应物获得能量在生成物中储存的过程,常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、工业制水煤气、碳(一氧化碳、氢气)还原金属氧化物、某些复分解(如铵盐和强碱).
A.燃烧为放热反应;
B.原子结合形成分子是化学键形成属于放热过程;
C.分解反应一般属于吸热反应,有的分解反应也是放热反应;
D.灼热的碳与二氧化碳反应属于吸热反应;
解答 解:A.燃甲烷烧为放热反应,故A错误;
B.原子结合形成分子是化学键形成,形成化学键的过程属于放热过程;,故B错误
C.分解反应一般属于吸热反应,有的分解反应也是放热反应,如2HI分解反应为放热反应,故C错误;
D.灼热的碳与二氧化碳反应属于吸热反应,故D正确;
故选D.
点评 本题考查学生对吸热反应的含义的理解,当反应物的能量低于生成物总能量时,反应是吸热反应,题目难度不大.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
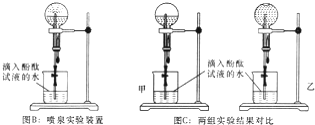
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子在1s轨道上运动像地球围绕太阳旋转 | |
| B. | 2s的电子云半径比1s电子云半径大,说明2s能级的电子比1s的多 | |
| C. | 1s轨道的电子云形状为圆形的面 | |
| D. | nf能级中最多可容纳14个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
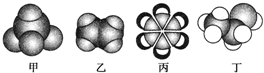
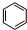 ,丁CH3CH2OH
,丁CH3CH2OH +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$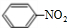 +H2O
+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
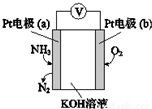
| A. | 该传感器在工作过程中KOH的物质的量不变 | |
| B. | a极的电极反应式为2NH3+3O2--6e-═N2+3H2O | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | b极为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,4.48L3717Cl2含有0.72NA个中子 | |
| B. | 3717Cl、3517Cl互为同位素,3717Cl2、3517Cl2互为同素异形体 | |
| C. | 通常情况下,氯气做氧化剂,但氯气也具有还原性 | |
| D. | 3717Cl2的摩尔质量是74 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 编号 | HA物质的量 浓度/(mol•L-1) | NaOH物质的量 浓度/(mol•L-1) | 混合后溶 液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH<7 |
| 丁 | 0.1 | 0.1 | pH=10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com