
| A. | NH4Cl的电子式: | |
| B. | HClO的结构式为:H-Cl-O | |
| C. | 氯化镁的电子式: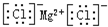 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
分析 A.氯离子的电子式没有标出最外层电子;
B.次氯酸的中心原子为O原子,分子中不存在H-Cl键;
C.氯化镁为离子化合物,阴阳离子需要标出所带电荷,氯离子需要标出最外层电子;
D.HCl为共价化合物,不存在阴阳离子.
解答 解:A.氯化铵是离子化合物,由氨根离子与氯离子构成,氯化铵正确的电子式为 ,故A错误;
,故A错误;
B.次氯酸分子中含有1个H-O键和1个O-Cl键,其正确的结构式为:H-O-Cl,故B错误;
C.氯化镁的电子式中,镁离子直接用离子符号表示,氯离子需要标出所带电荷及最外层电子,氯化镁的电子式为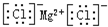 ,故C正确;
,故C正确;
D.氯化氢是共价化合物,不存在离子键,氢原子与氯原子之间形成1对共用电子对,氯原子最外层有7个电子,氯化氢分子的形成过程 ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、结构简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的分析能力及灵活应用能力.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 煤、石油等化石燃料燃烧过程中排放的废气是形成酸雨的主要原因,酸雨指的是pH小于7的雨水 | |
| B. | 雾霾可能是许多细小液体和固体微粒分散到空气中形成的一种气溶胶 | |
| C. | 在煤中添加适量的石膏可减少燃烧过程中含硫化合物的排放从而减少污染 | |
| D. | 煤和石油都属于一级能源而天然气属于二级能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱性氧化物:Na2O、CaO、Al2O3、H2O | B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | ||
| C. | 氧化物:Fe2O3、NO、SO2、CuO | D. | 酸:H2SO4、HNO3、NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
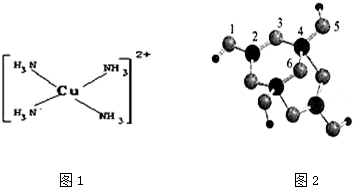
| A. | (1)(2)(3)(4)(5) | B. | (4)(5)(7)) | C. | (4)(5) | D. | (3)(4)(5)(7) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
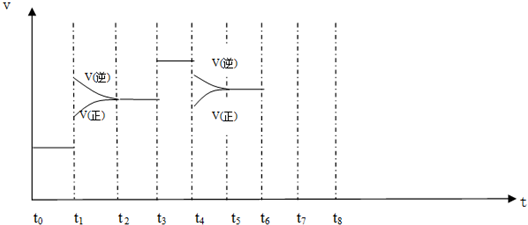
| A. | 达到化学反应限度时,可生成2mol NH3 | |
| B. | 向容器中再加入N2,可以加快反应速率 | |
| C. | 降低温度可以加快反应速率 | |
| D. | 1mol N2 和3mol H2的总能量低于2mol NH3的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水溶性:乙醇>新戊烷>苯酚 | |
| B. | 同质量的物质燃烧消耗O2量:乙烷>甲烷>乙炔 | |
| C. | 密度:水>苯>硝基苯 | |
| D. | 沸点:正戊烷>异戊烷>新戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
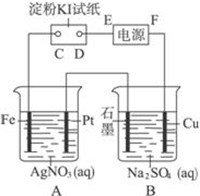 室温下,用下图所示的装置进行电解.通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色.若电解结束时,A、B装置中共收集到气体1.68L(标准状况),假设电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000mL,求此时A溶液的pH值.(提示:pH=-lgc(H+))
室温下,用下图所示的装置进行电解.通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色.若电解结束时,A、B装置中共收集到气体1.68L(标准状况),假设电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000mL,求此时A溶液的pH值.(提示:pH=-lgc(H+))查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com