
| A. | 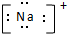 | B. |  | C. |  | D. |  |
科目:高中化学 来源: 题型:多选题
| A. | 同周期的IA族元素的金属性比IIA族的元素金属性强 | |
| B. | 第三周期元素的阴离子半径从左到右逐渐减小 | |
| C. | VIA族的气态氢化物一定比VA族的稳定性强 | |
| D. | 原子晶体的熔点一定比离子晶体的高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH | B. | CH3COOH | C. | CH3COOCH2CH3 | D. | CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾水解形成胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 现代建筑的门框架,常用古铜色的硬铝制造,硬铝含有的元素是Al、Cu、Mg等 | |
| C. | 金属在自然界中一般以化合态存在,越活泼的金属越难冶炼 | |
| D. | 日常生活中应用的金属材料一般为合金,合金的熔点一般比组分金属高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③>②>①>④ | B. | ②>③>④>① | C. | ②>③>①>④ | D. | ①>③>④>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入硝酸酸化的硝酸银溶液,有白色沉淀产生,一定有Cl- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润蓝色石蕊试纸变红,一定有NH4+ | |
| D. | 用铂丝蘸取某溶液在酒精灯火焰上灼烧,火焰呈黄色,说明原溶液中一定不含有K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:MnO2熔融氧化:3MnO2+KClO3+6KOH $\frac{\underline{\;熔融\;}}{\;}$3K2MnO4+KCl+3H2O;K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3.
高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:MnO2熔融氧化:3MnO2+KClO3+6KOH $\frac{\underline{\;熔融\;}}{\;}$3K2MnO4+KCl+3H2O;K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com