
【题目】不同元素的原子在分子内吸引电子的能力大小可用一数值X来表示,若X越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。下面是某些短周期元素的X值。
元素 | Li | Be | B | C | O | F |
X值 | 0.98 | 1.57 | 2.04 | 2.53 | 3.44 | 3.98 |
元素 | Na | Al | Si | P | S | Cl |
X值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析X值的变化规律,确定N、Mg的X值范围:___<X(Mg)<___;___<X(N)<___。
(2)推测X值与原子半径的关系是___。
(3)某有机物结构简式为![]() ,在SN中,你认为共用电子对偏向谁?___(写原子名称)。
,在SN中,你认为共用电子对偏向谁?___(写原子名称)。
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是_______。
(5)预测元素周期表中,X值最小的元素位置_______(放射性元素除外)。
【答案】0.93 1.57 2.55 3.44 同周期(或同主族)元素,X值越大,原子半径越小, 氮 共价键 第六周期第ⅠA族
【解析】
(1)由表中数值可看出,同周期中元素的X值随原子半径的减小而增大,同主族自上而下X值减小,X值的变化体现周期性的变化,故:0.93<X(Mg)<1.57,2.55<X(N)<3.44,
故答案为:0.93;1.57;2.55;3.44;
(2)由表中数值可看出,同周期中元素的X值随原子半径的减小而增大,同主族自上而下原子半径增大,而X值减小,
故答案为:同周期(或同主族)元素,X值越大,原子半径越小;
(3)对比周期表中对角线位置的X值可知:X(B)>X(Si),X(C)>X(P),X(O)>X(Cl),则可推知:X(N)>X(S),所以SN中,共用电子对应偏向氮原子,
故答案为:氮;
(4)查表知:AlCl3的△X=3.16-1.61=1.55<1.7,又X(Br)<X(Cl),所以AlBr3的△X应小于AlCl3的,为共价键,
故答案为:共价键;
(5)根据递变规律,X值最小的应为Cs(Fr为放射性元素)位于第六周期、第ⅠA族,
故答案为:第六周期第ⅠA族。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.100 mol·L-1的NaOH溶液分别逐滴加入到20.00 mL 0.100 0 mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确的是( )
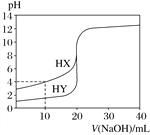
A. V(NaOH)=10.00 mL时,两份溶液中c(X-)>c(Y-)
B. V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
C. V(NaOH)=20.00 mL时,c(OH-)>c(H+)>c(Na+)>c(X-)
D. pH=7时,两份溶液中c(X-)=c(Na+)=c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学实验”进课堂,某化学教师为氯气与金属钠反应设计了如下装置与操作以替代相关的课本实验。实验操作:钠与氯气反应的装置作如下图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是( )
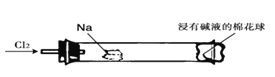
A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C. 钠着火燃烧产生苍白色火焰
D. 若在棉球外沿滴一滴淀粉碘化钾溶液,据其颜色变化判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(含氧化铝、氧化铁)制取金属铝的生产过程如下框图

请回答下列问题:
(1)纯净的氧化铝俗称____________,属于____________晶体。写出铝土矿与氢氧化钠溶液反应的离子方程式_______________。
(2)沉淀C的化学式为______,该物质除了用于金属冶炼以外,还可用作______________。电解熔融的氧化铝时,物质α是______,其作用是_________________。
(3)在实验室中欲从溶液E中得到较纯净的固体NaOH,需要进行的操作顺序是:_______、趁热过滤、____、__________。
(4)生产过程中,可以循环使用的物质有四种,除NaOH、H2O、CaO、CO2。其中NaOH中含有的化学键是______、________(如有共价键须标明极性还是非极性)。CaO、CO2的电子式分别为_____、____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应方程式如下,完成相应问题
___Fe3++___SO2+___H2O→___Fe2++___SO42-+___H+
(1)配平上述反应方程式并标出电子转移的方向和数目__________。
(2)反应中氧化剂为________,还原剂为________。
(3)反应中,所得氧化产物和还原产物的物质的量之比为_____________。
(4)反应过程中,溶液颜色由_______变为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铝铵![]() 是一种重要的分析试剂,下列有关说法正确的是( )
是一种重要的分析试剂,下列有关说法正确的是( )
A.硫酸铝铵中![]() 的水解程度比明矾中
的水解程度比明矾中![]() 的水解程度大
的水解程度大
B.该物质的水溶液中![]() 、
、![]() 、
、![]() 、
、![]() 都可大量共存
都可大量共存
C.向该物质的溶液中滴加同浓度的NaOH溶液的体积与生成沉淀的关系如图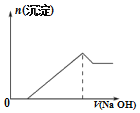
D.向该物质的溶液中滴加![]() 溶液,使
溶液,使![]() 恰好完全沉淀的离子方程式为:
恰好完全沉淀的离子方程式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是
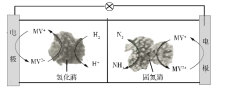
A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区,在氢化酶作用下发生反应H2+2MV2+![]() 2H++2MV+
2H++2MV+
C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D. 电池工作时质子通过交换膜由负极区向正极区移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按以下步骤可从![]() 合成
合成 ![]() (部分试剂和反应条件已去).
(部分试剂和反应条件已去).

请回答下列问题:
(1)A的名称为__________。
(2)分别写出 B、F 的结构简式:B_____、F_____。
(3)反应①~⑦中属于消去反应的是_____,属于加成反应的是_____(填代号)。
(4)根据反应![]() +Br2
+Br2![]() ,写出在同样条件下CH2=CH—CH=CH2 与等物质的量Br2反应的化学方程式:__________________。
,写出在同样条件下CH2=CH—CH=CH2 与等物质的量Br2反应的化学方程式:__________________。
(5)写出第④步的化学方程式_______________。
(6)下列有机物分子中,在核磁共振氢谱图中能给出三种峰(信号)且强度之比为 1∶1∶2 的是_______________。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴入某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:![]() ]。下列叙述不正确的是
]。下列叙述不正确的是

A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液的过程中,![]() 保持不变
保持不变
C. m点所示溶液中:c(H+)+c(Na+)=c(HA)+c(OH-)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com