
【题目】除去甲烷中混有的乙烯
A. 酸性高锰酸钾溶液B. 溴水C. 溴的四氯化碳溶液D. 氢氧化钠溶液
科目:高中化学 来源: 题型:
【题目】用50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 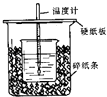
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 .
(2)烧杯间填满碎纸条的作用是 .
(3)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大、偏小、无影响”)
(4)如果用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等、不相等”),所求中和热(填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
药品名称 | 熔点/℃ | 沸点(℃) | 密度g/cm3 | 溶解性 |
丁醇 | ﹣89.5 | 117.7 | 0.8098 | 微溶于水、溶于浓硫酸 |
1﹣溴丁烷 | ﹣112.4 | 101.6 | 1.2760 | 不溶于水和浓硫酸 |
根据题意完成填空:
(一)制备1﹣溴丁烷粗产品:在下图装置的圆底烧瓶中依次加入NaBr,10mL正丁醇,2粒沸石,分批加入1:1的硫酸溶液,摇匀,加热30min.化学方程式:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O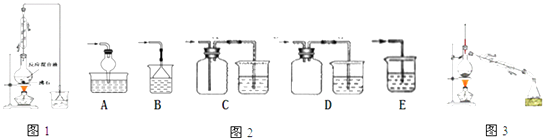
(1)图1反应装置中加入沸石的目的是 . 配制体积比为1:1的硫酸所用的定量仪器为(选填编号) a.天平 b.量筒 c.容量瓶 d.滴定管
(2)冷凝管的进水方向为 , 这样选择的原因是 .
(3)图2装置中,能代替上图中最后收集装置的是(填序号).
(4)若用浓硫酸进行实验,有机层中会呈现棕黄色,除去其中杂质的正确方法是选填编号). a.蒸馏 b.氢氧化钠溶液洗涤 c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
(5)(二)制备精品:将得到的粗1﹣溴丁烷依次用浓硫酸、水、10% 碳酸钠、水洗涤后加入无水氯化钙进行干燥,然后再将1﹣溴丁烷按图3装置蒸馏. 收集产品时,控制的温度应在℃ 左右;
(6)实验制得的1﹣溴丁烷的质量为10.895g,则正丁醇的产率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 如果存放有钠、电石等危险化学品的仓库着火,消防员不能用水灭火,应用泡沫灭火器灭火
B. 用石英制成光导纤维,由水玻璃制硅胶都是化学变化
C. 利用油脂在碱性条件下的水解,可以制得肥皂和甘油
D. 糖类、油脂、蛋白质都是高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式,正确的是
A.Fe溶于稀盐酸:2Fe+6H+ = 2Fe3+ + 3H2↑
B.用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O
C.用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu=Fe2++Cu2+
D.铝与浓氢氧化钠溶液反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1 mol任何气体的体积都是22.4 L
B. 1 mol H2的质量是1 g,它所占的体积是22.4 L
C. 在标准状况下,1 mol任何物质所占的体积都约是22.4 L
D. 在标准状况下,1 mol任何气体所占的体积都约是22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数,下列叙述正确的是( )
A.0.5 mol Al与足量盐酸反应转移电子数为NA
B.标准状况下,22.4 L氨气与22.4 L氮气所含原子数均为2 NA
C.7.8gNa2O2所含的离子数为0.3NA
D.11.2LCl2完全溶于NaOH溶液,电子转移数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水水资源的利用和海水化学资源的利用具有非常广阔的前景。下列有关叙述不正确的是
A.海带灼烧后的灰烬中碘元素以I2形式存在
B.从海水中制得的氯化钠可以用于生产漂白粉
C.以淡化后的浓海水为原料可以提高制溴的效益
D.淡化海水的方法有蒸馏法、电渗析法、离子交换法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com