
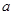 L含硫酸铵、硝酸铵的混合溶液分成两等份,一份用
L含硫酸铵、硝酸铵的混合溶液分成两等份,一份用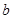 mol烧碱刚好把NH3全部赶出,另一份与氯化钡溶液完全反应消耗
mol烧碱刚好把NH3全部赶出,另一份与氯化钡溶液完全反应消耗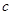 molBaCl2,则原溶液中
molBaCl2,则原溶液中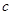 (NO
(NO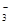 )为( )
)为( )A.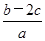 mol·L-1 mol·L-1 | B.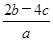 mol·1-1 mol·1-1 |
C. mol·L-1 mol·L-1 | D.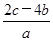 mol·L-1 mol·L-1 |
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源:不详 题型:单选题
| A.a=b/3 | B.2a=b | C.a≥b | D.a<b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硫具有漂白性,因而通入紫色石蕊试液中先变红后褪色 |
| B.浓硫酸和浓硝酸在常温下均可迅速与铜片反应放出气体 |
| C.浓硫酸与亚硫酸钠反应制备二氧化硫时,浓硫酸表现强氧化性 |
| D.稀硫酸和稀硝酸都具有氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.h1>h2>h3 | B.h1>h3>h2 | C.h2>h3>h1 | D.h3>h1>h2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.平面三角形,键角小于120° |
| B.平面三角形,键角为120° |
| C.三角锥形,键角小于109°28′ |
| D.三角锥形,键角为109°28′ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

 2NH3,该反应在固定容积的密闭容器中进行。
2NH3,该反应在固定容积的密闭容器中进行。| A.容器内N2、H2、NH3的浓度之比为l:3:2 |
B. |
| C.容器内压强保持不变 |
| D.混合气体的密度保持不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) ;△H< 0 。 400℃、30MPa下n(NH3)和n(H2)随时间变化的关系如图,下列叙述错误的是( )
2NH3(g) ;△H< 0 。 400℃、30MPa下n(NH3)和n(H2)随时间变化的关系如图,下列叙述错误的是( )
| A.点a的正反应速率比b点的大 |
| B.点c处反应还未达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D.其他条件不变,500℃下反应至t1时刻, n(H2)比右图中d点的值大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com