
| m |
| M |
| 5.4g |
| 18g/mol |
| 8.8g |
| 44g/mol |
| 6.2g-3g |
| 16g/mol |
| 62 |
| 31 |
| 9.2g |
| 23g/mol |
| 0.4mol |
| 0.2mol |


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 化合物中各元素的原子个数比 | A:C=1:1 | B:A=1:2 | D:C=1:1 | E:F=1:3 | B:F=1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
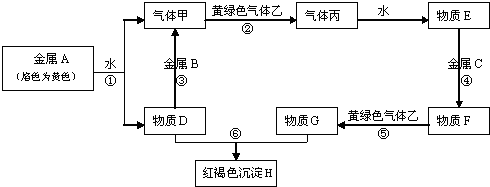
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
查看答案和解析>>
科目:高中化学 来源: 题型:
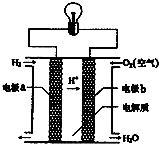
| A、a极是正极,b极是负极 |
| B、该装置能将化学能转化为电能 |
| C、电子由a极通过导线流向b极 |
| D、供电时总反应为2H2+O2=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5种 | B、6种 | C、7种 | D、8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Xm+的半径大于Yn-的半径 |
| B、X和Y处在同一周期 |
| C、Y和X的族序数之差是8-m-n |
| D、X和Y的核电荷数之差是m-n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com