
| 混合物成分 | 提纯试剂 | 离子方程式 |
| ①FeCl2溶液(FeCl3) | ||
| ②FeCl3溶液(FeCl2) | ||
| ③Na2CO3溶液(NaHCO3) | ||
| ④Fe2O3(Al2O3) |
分析 ①Fe与氯化铁反应生成氯化亚铁;
②氯气与氯化亚铁反应生化池氯化铁;
③碳酸氢钠与NaOH溶液反应生成碳酸钠;
④氧化铝与NaOH溶液反应,而氧化铁不能,以此来解答.
解答 解:①Fe与氯化铁反应生成氯化亚铁,试剂为Fe,离子反应为Fe+2Fe3+═2Fe2+;
②氯气与氯化亚铁反应生化池氯化铁,试剂为Cl2,离子反应为2Fe2++Cl2═2Fe3++2Cl-;
③碳酸氢钠与NaOH溶液反应生成碳酸钠,试剂为NaOH,离子反应为HCO3-+OH-=CO32-+H2O;
④氧化铝与NaOH溶液反应,而氧化铁不能,试剂为NaOH,离子反应为Al2O3+2OH-=2AlO2-+H2O,
故答案为:
| 混合物成分 | 提纯试剂 | 离子方程式 |
| ①FeCl2溶液(FeCl3) | Fe | Fe+2Fe3+═2Fe2+ |
| ②FeCl3溶液(FeCl2) | Cl2 | 2Fe2++Cl2═2Fe3++2Cl- |
| ③Na2CO3溶液(NaHCO3) | NaOH | HCO3-+OH-=CO32-+H2O |
| ④Fe2O3(Al2O3) | NaOH | Al2O3+2OH-=2AlO2-+H2O |
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
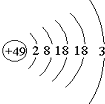 张青莲是我国著名的化学家.1991年,他准确测得In的相对原子质量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中首次采用我国测定的相对原子质量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
张青莲是我国著名的化学家.1991年,他准确测得In的相对原子质量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中首次采用我国测定的相对原子质量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )| A. | In为长周期元素 | B. | In为过渡金属元素 | ||
| C. | In容易导电导热 | D. | In在反应中容易失电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
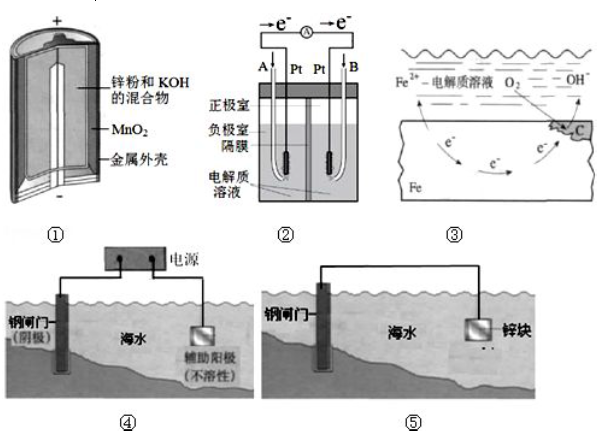
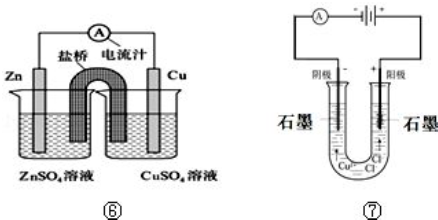
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg和Al | B. | Al和Fe | C. | Fe和Cu | D. | Na和Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2SO2(g)+O2?2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量 | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知H+(aq)+OH-(aq)═H2O(1)△H=-57.3kJ•mol-1,则任何酸碱中和的反应热均为57.3kJ | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1,2C(s)+O2(g)═2CO(g)△H2;则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Mg2+、OH-、Cl- | B. | Ba2+、K+、SO42-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、Cl- | D. | Na+、Al3+、Cl-、AlO2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com