
| A. | vA=0.5 mol•L-1•s-1 | B. | v B=0.5 mol•L-1•s-1 | ||
| C. | vC=0.4 mol•L-1•s-1 | D. | vD=1.2 mol•L-1•min-1 |
分析 把单位统一成相同单位,再根据各物质的反应速率之比等于其计量数之比,先把不同物质的反应速率换算成同一物质的反应速率进行比较,从而确定选项.
解答 解:对于反应3A(g)+B(g)═2C(g)+2D(g),都转化为A表示的速率进行比较,
A.vA=0.5 mol•L-1•s-1;
B.v B=0.5 mol•L-1•s-1,vA=3v B=1.5 mol•L-1•s-1;
C.v C=0.4 mol•L-1•s-1,vA=1.5v C=0.6 mol•L-1•s-1;
D.vD=1.2 mol•L-1•min-1=0.02 mol•L-1•s-1,vA=1.5v D=0.03 mol•L-1•s-1,
故选B.
点评 本题考查化学反应速率快慢比较,难度不大,注意对对化学反应速率及其表示法的理解及应用,也可以利用比值法进行比较,注意单位是否相同.


科目:高中化学 来源: 题型:填空题
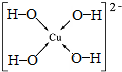 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能燃烧生成二氧化碳和水 | B. | 能跟溴水发生加成反应 | ||
| C. | 能跟酸性KMnO4溶液发生氧化反应 | D. | 能与氯化氢反应生成氯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B<C<A | B. | A<B<C | C. | C<B<A | D. | B>C>A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
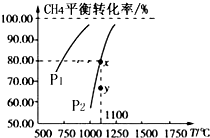 在一恒容的密闭容器中充入0.1mol/L CO2、0.1mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡转化率与温度、压强关系如图,下列有关说法不正确的是( )
在一恒容的密闭容器中充入0.1mol/L CO2、0.1mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡转化率与温度、压强关系如图,下列有关说法不正确的是( )| A. | 此条件下,1molCH4(g)和1molCO2(g)的总能量大于2mol CO(g)和2molH2(g)的总能量 | |
| B. | 压强:P2>P1 | |
| C. | 1100℃达平衡时,c(CO)=0.16 mol/L | |
| D. | 压强为P2时,在y点:v正>v逆 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Al2O3(熔融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑ | B. | Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3 | ||
| C. | Fe+CuSO4═FeSO4+Cu | D. | MgCl2(水溶液)$\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
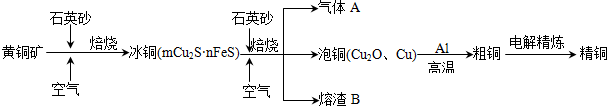
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com