
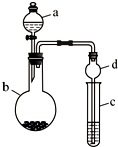
 某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验.请根据下列实验回答问题:
某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验.请根据下列实验回答问题: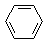 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$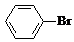 +HBr.向c中滴加AgNO3溶液,可观察到的现象是产生浅黄色沉淀.
+HBr.向c中滴加AgNO3溶液,可观察到的现象是产生浅黄色沉淀.分析 (1)验证物质的氧化性:KMnO4>Cl2>Br2,a中加浓盐酸,b中加KMnO4,发生2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,c中为含溴离子的化合物,c中发生2Br-+Cl2=2Cl-+Br2,结合氧化剂的氧化性大于氧化产物的氧化性可验证;
(2)a中盛液溴,b中为铁屑和苯,发生取代反应生成溴苯和HBr,HBr易溶于水,与硝酸银反应生成AgBr沉淀;
(3)a中加浓硫酸,b中盛装乙醇和乙酸,发生酯化反应生成乙酸乙酯,c中饱和碳酸钠溶液可除去乙醇、乙酸,与乙酸乙酯分层.
解答 解:(1)a中加浓盐酸,b中加KMnO4,发生2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,c中为NaBr或KBr,c中发生2Br-+Cl2=2Cl-+Br2,由氧化剂的氧化性大于氧化产物的氧化性可知,物质的氧化性为KMnO4>Cl2>Br2,c中生成溴不易溶于水,易溶于有机溶剂,则向c中加入少量CCl4,振荡静置后观察到c中的现象为液体分层,上层无色,下层为橙红色,
故答案为:NaBr或KBr;2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O;液体分层,上层无色,下层为橙红色;
(2)a中盛液溴,b中为铁屑和苯,发生取代反应生成溴苯和HBr,涉及的反应为2Fe+3Br2═2FeBr3、
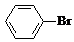
故答案为:2Fe+3Br2═2FeBr3;
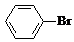
(3)a中加浓硫酸,b中盛装乙醇和乙酸,发生酯化反应生成乙酸乙酯,反应为CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,c中应盛装饱和Na2CO3溶液,其作用为除去乙酸乙酯中混有的乙酸和乙醇,故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;饱和Na2CO3;除去乙酸乙酯中混有的乙酸和乙醇.
点评 本题考查较为综合,涉及物质的性质实验和制备实验,注重高频考点的考查,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及题给信息,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 能燃烧生成二氧化碳和水 | B. | 能跟溴水发生加成反应 | ||
| C. | 能跟酸性KMnO4溶液发生氧化反应 | D. | 能与氯化氢反应生成氯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Al2O3(熔融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑ | B. | Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3 | ||
| C. | Fe+CuSO4═FeSO4+Cu | D. | MgCl2(水溶液)$\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃20 mL 3 mol/L的盐酸 | B. | 10℃40 mL 2 mol/L的盐酸 | ||
| C. | 20℃20 mL 2 mol/L的盐酸 | D. | 20℃10 mL 4 mol/L的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将红热的铜丝迅速插入乙醇中,可观察到铜丝表面变红,并能闻到刺激性气味 | |
| B. | 乙醇(CH3CH2OH)与二甲醚(CH3-O-CH3)互为同分异构体 | |
| C. | 在蛋白质溶液中加入饱和硫酸铵溶液,会使蛋白质发生变性 | |
| D. | 煤的干馏是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
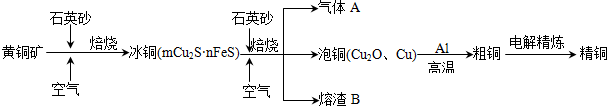
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
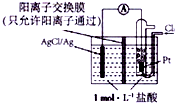
| A. | 正极为Pt电极,电极反应为2Ag++Cl2+2e-═2AgCl↓ | |
| B. | 放电时,交换膜两侧溶液中盐酸浓度不变 | |
| C. | 若用NaCl溶液代替盐酸,则电池总反应随之改变 | |
| D. | 当电路中转移0.01mole-时,交换膜左侧溶液中约减少0.02mol离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com