
设nA为阿伏伽德罗常数的数值,下列说法正确的是( )
A. 1mol Fe与足量的盐酸反应,转移3nA个电子
B. 0.1mol•L﹣1的NaNO3溶液中含有0.1nA个NO3﹣
C. 常温下,34gNH3含有2nA个NH3分子
D. 常温常压下,22.4LNO2含有2nA个氧原子
考点: 阿伏加德罗常数.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A、1mol铁与盐酸反应生成的是亚铁离子失去2mol电子;
B、溶液体积不明确;
C、求出氨气的物质的量,然后根据分子个数N=nNA来计算;
D、常温常压下,气体摩尔体积大于22.4L/mol.
解答: 解:A、1mol铁与盐酸反应生成的是亚铁离子失去2mol电子,故转移2mol电子,即2nA个,故A错误;
B、溶液体积不明确,故溶液中NO3﹣的个数无法计算,故B错误;
C、34g氨气的物质的量n=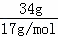 =2mol,而分子个数N=n•nA=2nA,故C正确;
=2mol,而分子个数N=n•nA=2nA,故C正确;
D、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L二氧化氮的物质的量小于1mol,则含有的氧原子的个数小于2nA,故D错误.
故选C.
点评: 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的运用以及物质的状态和结构是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
已知反应A2(g)+2B2(g)
 2AB2(g) ΔH<0,下列说法正确的是( )
2AB2(g) ΔH<0,下列说法正确的是( )
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)现有下列状态的物质①干冰 ②NaCl晶体 ③氨水 ④醋酸 ⑤酒精水溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖,其中属于电解质的是 (填序号),属于非电解质的是 (填序号),能导电的是 (填序号).
(2)某有色电解质溶液中,可能大量存在有Ag+、H+、Cu2+、OH﹣、Cl﹣等离子,你认为:一定有的离子是 ,一定没有的离子是 ,不能确定的离子 .
查看答案和解析>>
科目:高中化学 来源: 题型:
对可逆反应2A(s)+3B(g)C(g)+2 D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v (正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①② B.④ C.③ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
密闭容器中发生如下反应:A(g)+3B(g)2C(g) ΔH<0,根据下列速率—时间图象,回答下列问题:
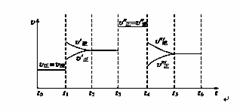
(1)产物C的体积分数最大的时间段是________;
(2)上述图象中C的体积分数相等的时间段是________;
(3)反应速率最大的时间段是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组顺序的排列不正确的是( )
A. 碱性强弱:NaOH>Mg(OH)2>Al(OH)3
B. 热稳定性:HF>HCl>H2S>PH3
C. 微粒半径:Na+>Mg2+>Al3+>F﹣
D. 熔点:SiO2>NaCl>I2>CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
在1.01KPa和298K条件下,2molH2生成水蒸汽放出484kJ热量,下列热化学方程式正确的是( )
A. 2H2(g)+O2(g)=2H2O(l);△H=﹣484kJ/mol
B. H2O(g)=H2(g)+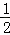 O2(g);△H=﹣242kJ/mol
O2(g);△H=﹣242kJ/mol
C. 2H2(g)+O2(g)=2H2O(g);△H=+484kJ/mol
D. H2(g)+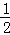 O2(g)=H2O(g);△H=﹣242kJ/mol
O2(g)=H2O(g);△H=﹣242kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A Cl2具有漂白性 Cl2能使干燥的有色布条褪色
B F元素非金属性很强 HF是一种强酸
C 浓H2SO4有强氧化性,SO2具有较强的还原性 但浓H2SO4却能干燥SO2
D 乙醇能杀菌消毒 医药上选用纯酒精进行消毒
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
|
| A. | 分散质颗粒直径都在l~100nm之间 |
|
| B. | 能透过半透膜 |
|
| C. | 加热蒸干、灼烧后都有氧化铁生成 |
|
| D. | 呈红褐色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com