
【题目】1,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用图9所示装置制备1,2二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。请填写下列空白:

(1)烧瓶a要求温度迅速升高到170℃发生反应,写出该反应的化学方程式 ;该反应类型为 。
(2)写出制备1,2二溴乙烷的化学方程式 。
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象 。
(4)容器c中NaOH溶液的作用是 ;e装置内NaOH溶液的作用是 。
(5)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因(至少2点) 、 。
【答案】(1)CH3CH2OH![]() CH2=CH2↑+H2O;消去反应(2)CH2=CH2+Br2 → CH2BrCH2Br
CH2=CH2↑+H2O;消去反应(2)CH2=CH2+Br2 → CH2BrCH2Br
(3)b中水面会下降,玻璃管中的水面会上升,甚至溢出
(4)除去乙烯中带出的酸性气体或答二氧化碳、二氧化硫 吸收挥发出来的溴,防止污染环境
(5)①乙烯发生(或通过液溴)速度过快 ②实验过程中,乙烯和浓硫酸的混合液没有迅速达到170℃
【解析】
试题(1)烧瓶a中乙醇和浓硫酸的混合液加热,温度迅速升高到170℃发生消去反应生成乙烯和水,该反应的化学方程式为CH3CH2OH![]() CH2=CH2↑+H2O;该反应类型为消去反应。
CH2=CH2↑+H2O;该反应类型为消去反应。
(2)乙烯与溴水发生加成反应生成1,2二溴乙烷,化学方程式为CH2=CH2+Br2 → CH2BrCH2Br。
(3) 若d中发生堵塞,则生成的气体无法排出,导致b中压强增大,所以b中水面会下降,玻璃管中的水面会上升,甚至溢出。
(4) 浓硫酸具有脱水性和强氧化性,在加热的情况下,乙醇与浓硫酸发生副反应生成二氧化碳、二氧化硫等酸性气体,二氧化硫能与溴水反应生成硫酸、氢溴酸。为了防止对制备1,2-二溴乙烷的干扰,容器c中NaOH溶液的作用是除去乙烯中带出的酸性气体或答二氧化碳、二氧化硫;液溴易挥发,制得的产物中含有有毒的溴蒸气,则e装置内NaOH溶液的作用是吸收挥发出来的溴,防止污染环境。
(5)所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,说明反应中有副反应发生(例如乙醇被浓硫酸氧化或生成乙醚等)或者乙醇挥发而损耗;也有可能是生成乙烯的速度过快,乙烯来不及和溴反应就被排入室外等。答案为①乙烯发生(或通过液溴)速度过快;②实验过程中,乙烯和浓硫酸的混合液没有迅速达到170℃


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. 常温下,反应C(s)+CO2(g)===2CO(g)不能自发进行,则该反应的ΔH>0
D. 同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物E是一种医药中间体,常用于制备抗凝血药,可以通过下图所示的路线合成:
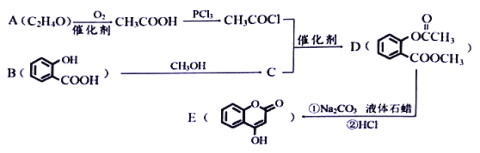
(1)有机物A结构简式为___________。B的名称为___________。
(2)C转化为D的反应类型是___________。
(3)写出E与足量NaOH溶液完全反应的化学方程式___________
(4)1moD完全水解且酸化后,所得有机物与足量 NaHCO3溶液反应生成CO2物质的量为___________。
(5)写出同时满足下列条件的C的同分异构体的结构简式___________。
①苯环上只有两个取代基,且除苯环外无其他环状结构
②核磁共振氢谱只有5个峰
③能与FeCl3溶液发生显色反应
④能水解并能与银氨溶液反应
(6)已知:酚羟基一般不易直接与羧酸酯化,甲苯可被酸性高锰酸钾溶液氧化为苯甲酸。试参照上述合成路线图,写出以苯酚、甲苯为原料制取苯甲酸苯酯(![]() )的合成路线(无机原料任选)___________。
)的合成路线(无机原料任选)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:

已知:①菱锰矿石主要成分是![]() ,还含有少量Fe、Al、Ca、Mg等元素;
,还含有少量Fe、Al、Ca、Mg等元素;
②相关金属离子![]() 形成氯氧化物沉淀时的pH如下:
形成氯氧化物沉淀时的pH如下:
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
③常温下, ![]() 的溶度积分别为
的溶度积分别为![]()
回答下列问题:
(1)“焙烧”时发生的主要化学反应方程式为_____________________。
(2)分析下列图1、图2、图3,氯化铵焙烧菱镁矿的最佳条件是:

焙烧温度_________,氯化铵与菱镁矿粉的质量之比为__________,焙烧时间为___________.
(3)浸出液“净化除杂”过程如下:首先加入![]() 氧化为
氧化为![]() ,反应的离子方程式为________;然后调节溶液pH使
,反应的离子方程式为________;然后调节溶液pH使![]() 沉淀完全,此时溶液的pH范围为____。再加入
沉淀完全,此时溶液的pH范围为____。再加入![]() 沉淀
沉淀![]() ,当
,当![]() 时,
时, ![]() =______
=______![]()
(4)碳化结晶时,发生反应的离子方程式为___________。
(5)流程中能循环利用的固态物质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒醛衍生物在香料、农药、医药等领域有着广泛用途,A为香草醛,以A为原料合成5-三氟甲基胡椒醛(E)的路线如图所示:

已知:
(1)反应①的类型是 。
(2)写出A中含氧官能团的名称 。
(3)写出反应③的化学方程式 。
(4)写出满足下列条件A的一种同分异构体的结构简式 。
①能与碳酸氢钠溶液反应放出气体
②不与氯化铁溶液发生显色反应
③含苯环,核磁共振氢谱显示其有5种不同化学环境的氢原子
(5)以A和2-氯丙烷为原料,可合成香草醛缩丙二醇( ),写出合成流程图(无机试剂任用)。合成流程图示例如下:
),写出合成流程图(无机试剂任用)。合成流程图示例如下:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A为一氯代物,H是通过缩聚反应获得的高聚物。

已知:![]() (苯胺,易被氧化)
(苯胺,易被氧化)
(1)X的结构简式为 。
(2)A的结构简式为 。
(3) G的结构简式为 。反应②③两步能否互换 ,(填“能”或“不能”)理由是 。
(4)反应④的化学方程式是 ;反应⑤的化学方程式是 。
(5)写出同时满足下列条件的阿司匹林的一种同分异构体的结构简式 。
①苯环上一卤代物只有2种;
②能发生银镜反应,分子中无甲基;
③1mol该物质最多能与3molNaOH反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子中质子、中子、电子的数量、质量和电性之间存在一定的相互关系。请填写下列空白:
(1)质子数决定________的种类;质子数和中子数决定________的种类。
(2)![]() 代表一个质量数为________、质子数为______、中子数为________、核外电子数为________的原子。
代表一个质量数为________、质子数为______、中子数为________、核外电子数为________的原子。
(3)质量数=________+________,对任一原子,核电荷数=________;对中性原子,核外电子数=________。
(4)ZXn-中核外电子数=________,ZXn+中核外电子数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传统中药的砷剂俗称“砒霜”,请回答下列问题:
(1)砷剂的分子结构如图甲所示.该化合物中As原子的杂化方式为__.
(2)基态砷原子的价层电子排布式为__,砷与硒的第一电离能较大的是__.
(3)已知:

依据表中数据解释NH3熔点最高的原因__.
(4)砷酸(H3AsO4)是一种三元中强酸,根据价层电子对互斥理论推测AsO43﹣的空间构型为__.
(5)砷镍合金的晶胞如图乙所示,该晶体中与每个Ni原子距离最近的As原子有__个.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,Ksp(Ag2SO4)=2.0×10-5。取适量Ag2SO4溶于蒸馏水得到200 mL饱和溶液,在该饱和溶液中c(SO42-)=0.017 mol·L-1。向该饱和溶液中加入0.020 mol·L-1 Na2SO4溶液200 mL,得到溶液R。(不考虑混合后溶液体积的变化)下列说法正确的是( )
A.R中c(Ag+)=2c(SO42-)
B.得到溶液R的过程中会产生沉淀
C.R中c(Ag+)=0.017 mol·L-1
D.加入Na2SO4溶液促进沉淀溶解平衡向左移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com