
| A. | 铁和稀盐酸反应:2 Fe+6H+═2Fe3++3 H2↑ | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 碳酸钙溶于稀盐酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 碳酸氢钠溶液中滴入NaOH溶液:HCO3-+OH-═H2O+CO2↑ |
分析 A.铁与稀盐酸反应生成的是亚铁离子;
B.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
C.碳酸钙与稀盐酸反应生成氯化钙、二氧化碳气体和水;
D.碳酸氢钠与氢氧化钠溶液反应生成碳酸钠和水.
解答 解:A.铁和稀盐酸反应生成氯化亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故A错误;
B.氯气与水反应生成氯化氢和次氯酸,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故B错误;
C.碳酸钙溶于稀盐酸中,反应的离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑,故C正确;
D.碳酸氢钠溶液中滴入NaOH溶液,反应生成的是碳酸钠和水,正确的离子方程式为:HCO3-+OH-═H2O+CO32-,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等,试题培养了学生的灵活应用能力.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将固体加热至不再有气体产生 | |
| B. | 将固体配成溶液,再加入过量的澄清石灰水 | |
| C. | 将固体配成溶液,再加入过量的NaOH溶液 | |
| D. | 将固体配成溶液,再通入足量的CO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C2H4O2的有机物不一定是乙酸 | |
| B. | 乙炔与足量Br2发生加成反应生成1,1,2,2-四溴乙烷 | |
| C. | 淀粉、蔗糖、葡萄糖在一定条件下都能发生水解反应 | |
| D. | 实验室用乙醇和浓H2SO4制备乙烯时,反应液体的温度要迅速上升到170℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由水电离的c(H+)=1×10-4 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| B. | 在pH=1的无色溶液中:Fe2+、Mg2+、NO3-、SO42- | |
| C. | c(K2C2O4)=1mol/L溶液中:Na+、Cl-、MnO4-、K+ | |
| D. | 能与铝反应产生H2的溶液中:Mg2+、SO42-、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
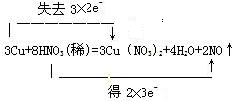 ;3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
;3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com