
| A. | CuCl2(CuCl2) | B. | AgNO3(Ag2O) | C. | NaCl(NaCl) | D. | CuSO4[Cu(OH)2] |
分析 用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质(括号内),溶液一定不能与原来溶液一样,说明加入物质不是析出物质,据此分析解答.
解答 解:A.电解氯化铜溶液时,阳极上氯离子放电、阴极上铜离子放电,所以析出的物质相当于氯化铜,则加入氯化铜即可恢复原状,故A不选;
B.电解硝酸银溶液时,阳极上氢氧根离子放电生成氧气、阴极上银离子放电生成Ag,相当于析出氧化银,所以加入氧化银即可使溶液恢复原状,故B不选;
C.电解氯化钠溶液时,阳极上析出氯气、阴极上析出氢气,要使溶液恢复原状,应该通入适量氯化氢即可,所以加入NaCl不能使溶液恢复原状,故C选;
D.电解硫酸铜溶液时,阳极上氢氧根离子放电生成氧气,阴极上铜离子放电生成Cu,当铜离子完全放电时,阴极上氢离子放电生成氢气,所以相当于析出氢氧化铜,应该加入氢氧化铜即可恢复原状,故D不选;
故选C.
点评 本题考查电解原理,为高频考点,明确离子放电顺序是解本题关键,根据“析出什么、加入什么”原则分析解答,易错选项是D,注意该选项是既电解硫酸铜还电解水,题目难度不大.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:选择题
| A. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| B. | 1.5molNO2与足量H2O反应,转移的电子数为1.5NA | |
| C. | 常温常压下,46gNO2和N2O4混合气体含有的原子数为3NA | |
| D. | 含有H2SO41mol的浓硫酸与足量铜反应,生成SO2的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2(SO4)3 | B. | NaOH | C. | Al2(SO4)3 | D. | BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | |
| Y | Z |
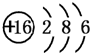 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  |  | [ 来源:] 来源:] |
| 向Ba(OH)2溶液中逐滴加入等浓度的H2SO4至过量 | 向醋酸溶液中逐滴加入等浓度的氨水至过量 | 向盐酸溶液中逐滴加入等浓度的NaOH溶液至过量 | 向氨水中逐滴加入等浓度的盐酸至过量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com