
分析 取0.3mol甲在足量氧气中完全燃烧后,生成1.5molCO2和1.8molH2O,则甲、C、H个数之比=0.3mol:1.5mol:3.6mol=1:5:12,该分子中含有5个C原子、12个H原子,因为80<Mr(甲)<100,所以O原子个数1,则甲的分子式为C5H12O;
甲的核磁共振氢谱有两个峰,说明含有两种氢原子,峰面积之比为3:1,说明两种类型的氢原子个数之比为3:1,所以甲的结构简式为(CH3)3COCH3.
解答 解:取0.3mol甲在足量氧气中完全燃烧后,生成1.5molCO2和1.8molH2O,则甲、C、H个数之比=0.3mol:1.5mol:3.6mol=1:5:12,该分子中含有5个C原子、12个H原子,因为80<Mr(甲)<100,所以O原子个数1,则甲的分子式为C5H12O,甲的相对分子质量=5×12+12×1+1×16=88;
甲的核磁共振氢谱有两个峰,说明含有两种氢原子,峰面积之比为3:1,说明两种类型的氢原子个数之比为3:1,所以甲的结构简式为(CH3)3COCH3;
(1)通过以上分析知,甲的分子式为C5H12O,故答案为:C5H12O;
(2)通过以上分析知,甲的结构简式为(CH3)3COCH3,故答案为:(CH3)3COCH3.
点评 本题考查有机物分子式的确定,为高频考点,把握原子守恒及H的种类为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
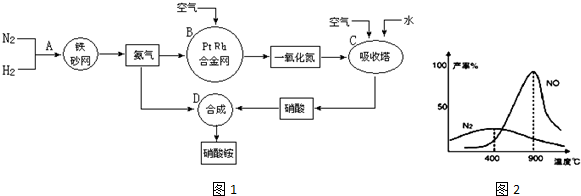
 4NO+6H2O,当温度高于900℃时,NO产率明显下降的原因是生成NO的反应为放热反应,升高温度转化率下降.
4NO+6H2O,当温度高于900℃时,NO产率明显下降的原因是生成NO的反应为放热反应,升高温度转化率下降.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石和石墨互为同素异形体 | |
| B. | CH3-CH2OH和 CH3-O-CH3互为同分异构体 | |
| C. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | |
| D. | 分子式为C4H10的物质为纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
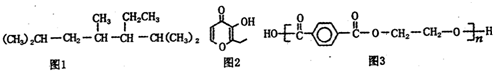
| A. | 按系统命名法命名,图1化合物的名称是2,4,6一三甲基-5-乙基庚烷 | |
| B. | 图2有机物的一种芳香族同分异构体能发生银镜反应 | |
| C. | 图2有机物能使酸性高锰酸钾溶液褪色 | |
| D. | 图3为髙分子化合物,其单体为对苯二甲酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
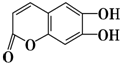 中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用.有机物M是中药狼把草的成分之一,其结构如图所示.下列叙述不正确的是( )
中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用.有机物M是中药狼把草的成分之一,其结构如图所示.下列叙述不正确的是( )| A. | M是芳香族化合物,它的分子式为C9H6O4 | |
| B. | 1 mol M最多能与3 mol Br2发生反应 | |
| C. | 1 mol M最多能与含有3 mol NaOH的溶液发生反应 | |
| D. | 在一定条件下能发生取代、加成、水解、氧化等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH的燃烧热为1452kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H>-571.6kJ/mol | |
| C. | 2CH3OH(l)+O2(g)═2CO2(g)+4H2(g)△H=-880.4kJ/mol | |
| D. | CH3COOH(aq)+NaOH(aq)═H2O(l)+CH3COONa(aq)△H=-57.3kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 8min时表示正反应速率等于逆反应速率 | |
| B. | 在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 | |
| C. | 40min时改变的条件是升高温度,且正反应为放热反应 | |
| D. | 反应方程式中的x=1,30min时改变的条件是降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3→Na++H++CO32- | B. | HClO→H++ClO- | ||
| C. | H2S?2H++S2- | D. | NH4++OH-→NH3•H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com