
| A. | 醋酸与锌反应放出的氢气多 | |
| B. | 盐酸和醋酸分别与锌反应放出的氢气一样多 | |
| C. | 醋酸与锌反应所需时间长 | |
| D. | 盐酸和醋酸分别与锌反应所需时间一样长 |
分析 pH均等于2的盐酸和醋酸,氯化氢是强电解质,醋酸是弱电解质,所以c(CH3COOH)>c(HCl),等pH等体积的盐酸和醋酸,n(CH3COOH)>n(HCl),盐酸和醋酸分别与足量锌反应时,酸的物质的量越多,生成氢气的量越大,酸与锌反应速率与氢离子浓度有关,氢离子浓度越大,反应速率越快,pH均等于2的盐酸和醋酸,加水稀释2倍后,醋酸溶液中氢离子浓度大于盐酸,pH均等于2的盐酸和醋酸溶液各100mL,含有氢离子物质的量为0.002mol,能够反应Zn的质量为0.065g,所以0.03gZn能够完全反应,生成氢气的量相同.
解答 解:A.pH均等于2的盐酸和醋酸溶液各100mL,含有氢离子物质的量为0.002mol,能够反应Zn的质量为0.065g,所以0.03gZn能够完全反应,生成氢气的量相同,故A才错误;
B.pH均等于2的盐酸和醋酸溶液各100mL,含有氢离子物质的量为0.002mol,能够反应Zn的质量为0.065g,所以0.03gZn能够完全反应,生成氢气的量相同,故B正确;
C.Zn能够完全反应,当pH=2的盐酸和醋酸稀释2倍后,醋酸中氢离子浓度大于盐酸,所以醋酸反应速率快,盐酸与锌反应所需时间长,故C错误;
D.当pH=2的盐酸和醋酸稀释2倍后,醋酸中氢离子浓度大于盐酸,所以醋酸反应速率大,盐酸与锌反应所需时间长,故D错误;
故选A.
点评 本题考查弱电解质电离,明确生成的氢气和酸的关系、反应速率和氢离子浓度关系即可解答,难度不大.


科目:高中化学 来源: 题型:解答题
| 方法1 | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫,其部分热化学方程式为: 2CO(g)+SO2(g)=S(g)+2CO2(g)△H=+8.0kJ•mol-1 2H2(g)+SO2(g)=S(g)+2H2O(g)△H=+90.4kJ•mol-1 |
| 方法2 | 用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸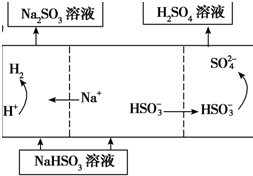 |
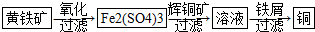
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
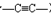 )组成的混合气体与足量的H2反应,充分加成后,生成4.4g3种对应的烷径中一定有( )
)组成的混合气体与足量的H2反应,充分加成后,生成4.4g3种对应的烷径中一定有( )| A. | 乙炔 | B. | 乙烷 | C. | 丙炔 | D. | 丙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学将为环境、能源、资源等问题的解决提供有力保障 | |
| B. | 化学正发展成为一门实验与理论互相结合、互相渗透的科学 | |
| C. | 化学是一门具有极强实用性的自然科学 | |
| D. | 化学是一门纯实验的自然科学,实验是探究化学过程的唯一途径 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;1124Na.
;1124Na.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
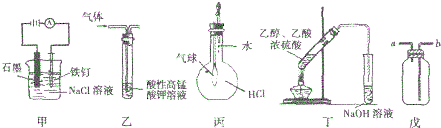
| A. | ③⑤ | B. | ③④ | C. | ①②④ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
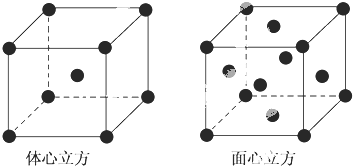
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用湿润的pH试纸测定某稀醋酸溶液的pH | |
| B. | 做完银镜反应的试管可以用氨水来洗涤 | |
| C. | 为了除去苯中混有的少量苯酚,加入足量浓溴水,充分搅拌后过滤分离 | |
| D. | 如果苯酚浓溶液沾到皮肤上,应立即用酒精擦洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
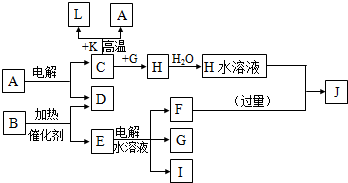
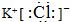 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com