
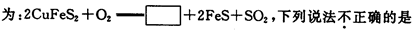
| A.方框中的物质应为 Cu2S | B.若有1 molSO2 生成,则反应中有4 mol 电子转移 |
| C.SO2既是氧化产物又是还原产物 | D.O2只作氧化剂 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 反应式可表示为:2NO2 +4CO ="==" N2 +4CO2
反应式可表示为:2NO2 +4CO ="==" N2 +4CO2 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
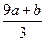 )mol
)mol| A.①④ | B.②④ | C.②③ | D.①③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.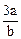 mol.L-1 mol.L-1 | B.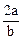 mol.L-1 mol.L-1 | C.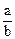 mol.L-1 mol.L-1 | D.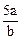 mol.L-1 mol.L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
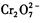 的废水的原理可概述为:向
的废水的原理可概述为:向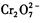 的酸性废水中加人FeSO4·7H2O ,将
的酸性废水中加人FeSO4·7H2O ,将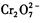 还原为Cr3+,调节溶液的 pH,使溶液中的铁、铬元素转化为组成相当于FeⅡ[FeⅢXCrⅢ 2-X]O4(铁氧磁体、罗马数字表示元素的价态)的沉淀。处理含 1 mol
还原为Cr3+,调节溶液的 pH,使溶液中的铁、铬元素转化为组成相当于FeⅡ[FeⅢXCrⅢ 2-X]O4(铁氧磁体、罗马数字表示元素的价态)的沉淀。处理含 1 mol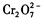 的废水至少需要加人amol FeSO4·7H2O 。下列结论正确的是 ( )
的废水至少需要加人amol FeSO4·7H2O 。下列结论正确的是 ( )| A.x= 0.5 , a=" 8" | B.x = 0.5 , a="10" | C.x = 1.5 , a=" 8" | D.x = 1.5 , a= 10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:1:1 | B.1:1:2 | C.2:2:1 | D.3:4:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com