
A、 检查容量瓶是否漏水 |
B、 给液体加热 |
C、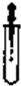 滴加液体 |
D、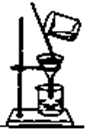 过滤 |
| 1 |
| 3 |
| 1 |
| 3 |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1-丁烯 |
| B、甲苯 |
| C、二甲苯 |
| D、2-甲基-3-乙基-2-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 连二亚硫酸钠(Na2S2O4)俗称保险粉,具有强还原性,广泛用于纺织品漂白及作脱氧剂等.
连二亚硫酸钠(Na2S2O4)俗称保险粉,具有强还原性,广泛用于纺织品漂白及作脱氧剂等.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钠溶液与少量石灰水反应 HCO3-+Ca2++OH-→CaCO3↓+H2O |
| B、Fe2(SO4)3的酸性溶液中通过入足量硫化氢:2Fe3++H2S→2Fe2++S↓+2H+ |
| C、浓盐酸与二氧化锰反应制氯气:MnO2+4H++2Cl-→Mn2++2H2O+Cl2↑ |
| D、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O→AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
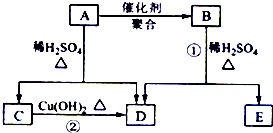 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如图所示:已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO.根据以上信息回答下列问题:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如图所示:已知R-CH=CHOH(烯醇)不稳定,很快转化为R-CH2CHO.根据以上信息回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2能使品红溶液褪色,是因为SO2具有漂白性 |
| B、SO2在空气中极易被氧化为SO3 |
| C、SO2通入Na2SO3或NaHCO3溶液中均能发生反应 |
| D、SO2是形成酸雨的大气污染物之一,主要来自于化石燃料的燃烧和工厂排放的废气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
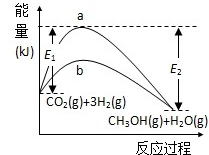 一定条件下发生反应:
一定条件下发生反应:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用水洗涤2~3次后再使用 |
| B、用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同再使用 |
| C、用盐酸洗涤,再用自来水洗净后使用 |
| D、用滤纸擦干净即可使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com